Поверхность - алюмосиликат
Cтраница 3
Донорные молекулы пиридина вытесняют радикал и с протонных и с апротонных кислотных центров. Oi этом свидетельствует уменьшение константы А и вкла да мультиплетного спектра при увеличении заполненш поверхности алюмосиликата пиридином. [31]
Результаты ультрамикроскопических, электронно-микроскопических и рентгеноскопических исследований [161, 167, 168] подтверждают предположение о том, что первопричиной флоку-лирующего действия ВМФ является адсорбционное закрепление концов макромолекул на твердых поверхностях. Большое значение принадлежит образованию водородных связей между недиссоциированной группой полимера и гидроксильными группами или атомами водорода на поверхности алюмосиликатов [ 104, 124 ( стр. [32]
Присутствие и роль этих катионов в кислотном катализе должна быть выяснена при дальнейшем исследовании. Небольшая часть всей связанной воды имеет существенное значение для активности катализатора, так как, вероятно, она служит источником протонов для кислотных центров поверхности алюмосиликата. Эти кислотные центры не активируются при воздействии на них неорганических и органических оснований. Дегидратированные кислотные центры часто называются льюисовскими кислотами. [33]
С - концентрация кокса, t - время, k - константа, зависящая от концентрации кислорода и температуры процесса. Выполненные расчеты показывают, что за равный промежуток времени с поверхности A1203 ( S 100м2 / г), содержащей 4 % кокга, удаляется столько же атомов углерода, сколько с поверхности алюмосиликата ( S 250м2 / г), содержащего 6 % кокса. Это, по-видимому, подтверждает предположение о том, что при таких концентрациях кокс покрывает поверхность катализатора монослоем. [34]
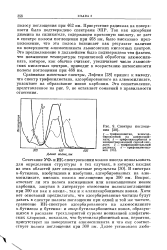 |
Спектры поглощения. [35] |
Присутствие радикала на поверхности было подтверждено спектрами ЭПР. Так как адсорбция диамина на силикагеле, содержащем протонную кислоту, не дает в спектре полосы поглощения при 468 нм, было высказано предположение, что эта полоса возникает как результат наличия на поверхности алюмосиликата льюисовских кислотных центров. Это предположение в дальнейшем было подтверждено тем фактом, что повышение температуры термической обработки алюмосиликата, которое, как обычно считают, увеличивает число льюисовских кислотных центров, приводит к возрастанию интенсивности полосы поглощения при 468 нм. [36]
Вначале мы обсудим метод селективного взаимодействия ряда реактивов с льюисовскими кислотными центрами, не затрагивающего бренстедовские. При изучении адсорбции антрацена и периле-на методом ЭПР и по спектрам поглощения Холл [65], Теренин и др. [66], Роберте и др. [67], Броуэр [68], Руни и Пинк [69] и Имелик и др. [70] обнаружили, что на поверхности алюмосиликата образуются ка-тион - р & дикалы, и объяснили их возникновение окислительным взаимодействием с кислотными Центрами Льюиса. Однако следует подчеркнуть разницу между центрами, принимающими один электрон - кислотными Центрами Льюиса в самом широком смысле, и теми Центрами, которые принимают пару электронов - собственно кислотными центрами Льюиса. [37]
Таким образом, кислота, которая может принять электронную пару для образования ковалептной связи, в результате присоединения молекул воды переходит в кислоту, способную отдавать протон. Гидроксильные группы на поверхности смешанных оксидов также проявляют разную реакционную способность. Например, - ОН-группы на поверхности алюмосиликата могут связываться с атомом кремния, с атомом алюминия и с катионом щелочного металла. Кроме того, на реакционной способности гидроксиль-ных групп сказывается взаимное вЛияние смешанных оксидов. [38]
 |
Обнаружение образования иона трифенилкарбония на алюмосиликате по ультрафиолетовому спектру ( Lef - tm И. P., J. Phys, Chem., 64, 1714 ( I960. [39] |
Спектр, полученный после адсорбции трифенилметана на алюмосиликате, соответствует спектру трифенилме-танола в концентрированной серной кислоте. При действии серной кислоты на указанный карбинол образуется трифенилметил-карбониевый ион. Этот ион стабилизируется и на поверхности алюмосиликата. Ион образуется из трифенилметана, вероятно, в результате реакции отщепления гидрид-иона ( см. разд. [40]
На электронно-микроскопических снимках образцов катализаторов с 0 6 - 1 0 % Pt, полученных пропиткой H2PtCle и восстановленных водородом при 670 К, Фигуерас и др. [58] наблюдали частицы платины размером от 2 до 10 нм. По-видимому, это объясняется повышенной неоднородностью поверхности алюмосиликатов, вызываемой поверхностными ионами алюминия, вблизи которых, как правило, скапливаются атомы металла, облегчая тем самым рост кристаллитов. С увеличением температур прокаливания и восстановления наблюдается тенденция к росту кристаллитов металла. [41]
Анализ этих данных показывает, однако, что в большинстве доказанных случаев неоднородной поверхности изучались процессы на поверхности катализаторов и адсорбентов, которые, по распространившейся за последнее время терминологии [4], относятся к электронному ( окислительно-восстановительном) типу. Данные о неоднородности поверхности по кислотно-основным свойствам почти отсутствуют в литературе. Исключение представляют лишь косвенные указания о наличии на поверхности алюмосиликатов кислотных центров разной каталитической активности [5-8], например, ионов водорода Н и алюминия Al: i. [42]
Изменение основности солей алюминия от A1 / NO3 2 до 4 не влияет на пористую структуру гранул цеолита. Это свидетельствует об одинаковом характере взаимодействия этих солей с поверхностью щелочного алюмосиликата. Раствор основной соли A1 ( OH) 2NO3, имеющий рН 1 5, частично разрушает кристаллы цеолита, вследствие чего структура и адсорбционные свойства продукта изменяются. Автор считает, что природа связующего оказывает очень большое влияние на архитектуру гранул. В случае продукта, полученного склеиванием с помощью глины, каркас гранулы образован сравнительно малопористыми частицами глины, которые частично экранируют поверхность кристаллитов цеолита. При склеивании основной солью связующее располагается главным образом в точках контакта кристаллов друг с другом, поэтому степень экранирования поверхности цеолитов в этом случае меньше. [43]
Метод ЭПР успешно применен при изучении адсорбции ароматических соединений на алшосиликатных катализаторах. Так, в работах советских и зарубеюых ученых было показано, что при адсорбции нафталина, перилена, антрацена, дифенилэтана на поверхности алюмосиликатных катализаторов, нагретых предварительно в вакууме или на воздухе, генерируются сигналы ЭПР с хорошо разрешенной сверхтонкой структурой. Сопоставление этих сигналов с соответствующими спектрами ароматических соединений в серной кислоте показывает, что адсорбированные на поверхности алюмосиликатов углеводороды представляют собой положительные ион-ра: пкалы. [44]
Метод ШР успешно применен при изучении адсорбции ароматических соединений на алюмосиликатных катализаторах. Так, в работах советских и зарубежных ученых было доказано что при адсорбции нафталина, перилена, антрацена, дифенилэтана на поверхности алюмосиликатных катализаторов, нагретых предварительно в вакууме или на воздухе, генерируются сигналы ШР о хорошо разрешенной сверхтонкой структурой. Сопоставление этих сигналов с соответствующими спектрами ароматических соединений в серной кислоте показывает, что адсорбированные на поверхности алюмосиликатов углеводороды представляют собой положительные ион-радикала. [45]
Страницы: 1 2 3 4