Поверхность - алюмосиликат
Cтраница 2
 |
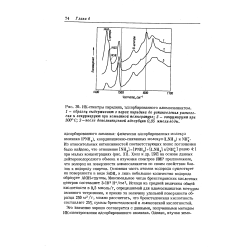
Низкотемпературная часть термограммы. [16] |
На основании работ А. В. Киселева [19, 20] и ряда исследователей по минералогии глин [1, 3, 19] можно считать, что на поверхности алюмосиликатов всегда имеются гидроксильные группы. Вермикулит, являющийся гидроалюмосиликатом, содержит, кроме молекулярной Н 0, связанной с поверхностью водородной связью, также большое количество ОН-групп. [17]
Холл и др. [56] на основе данных дейтероводородного обмена и изучения спектров ЯМР предположили, что водород на поверхности алюмосиликатов по своим свойствам близок к водороду спиртов. Основная часть атомов водорода существует на поверхности в виде SiOH, и лишь небольшое количество водорода образует АЮН-группы. Исходя из средней величины общей кислотности в 0 5 ммоль / г, определяемой для алюмосиликатов методом аминного титрования, и приняв за величину удельной поверхности образца 250 м2 / г, можно рассчитать, что бренстедовская кислотность составляет 25 % суммы бренстедовской и льюиеовской кислотностей. Это значение хорошо согласуется с данными, полученными методом ИК-спектроскопии адсорбированного аммиака. [19]
Результаты спектрального исследования [39] адсорбции n - фенилендиамина на алюмосиликате были интерпретированы как указание на присутствие льюисовских кислотных центров IT a поверхности алюмосиликата. Это соединение является донором электронов из-за присутствия несвязывающих электронов на атомах азота. [20]
В данном исследовании были использованы радиохимический метод, метод блокировки аммиаком и метод метки дейтерием для выяснения вопроса о том, какие центры на поверхности алюмосиликата ответственны за полимеризацию и изомеризацию бутена-1. По нескольким пунктам полученные результаты подтверждают опубликованные работы других исследователей. [21]
Количество введенных Na - ионов определялось как эквивалентное кислоте, выделившейся в раствор в результате обмена кислотного водорода алюмосиликатной структуры на ион натрия, и составляло после первой обработки 0 53 мг-экв / г, а после третьей - 0 91 мг-экв / г. Определение поверхности алюмосиликатов, модифицированных наггрием, дало величину 250 м2 / г. Таким образом, введение иаггрия в алюмосиликат гае ( изменило его удельной поверхности. [22]
В отличие от рассмотренной в разд. Поскольку поверхность алюмосиликатов гидрофильна, то в случае конденсации термодинамически более выгодно образование большого числа зародышей, и в результате - высокодисперсной системы, нежели образование малого числа крупных частиц. Вследствие развитой поверхности, в образующейся дисперсии ( конечно, при не слишком низких концентрациях) возникает большое количество контактов между частицами. Несовершенство кристаллической структуры алюмосиликатов и анизотропия свойств диспергированных частиц ( разные плотность / знак заряда на гранях и ребрах) приводят к выраженным агрегативным взаимодействиям частиц и образованию связнодисперсной системы за счет коагуляционных контактов. Если скорость седиментации меньше скоростей конденсации и коагуляции, то процесс гелеобразования преобладает над осаждением и уплотнением осадка. [23]
Однако Маркова ( 1961) получила спектр алюмосиликатного катализатора, содержащий три полосы поглощения гидроксильных групп. Очевидно, необходимы дальнейшие исследования поверхностей алюмосиликатов для определения мест присоединения гидроксильных групп к поверхности и выяснения причин частого отсутствия характерных для окиси алюминия полос поглощения гидроксильных групп. [24]
Этот раздел ограничивается рассмотрением силикагелей, в него не включены алюмосиликатные гели и катализаторы. Некоторые вопросы, связанные с поверхностью алюмосиликатов, обсуждаются в гл. [25]
Введение кремний-органических гидрофобизаторов позволяет повысить биостойкость поверхности щелочных алюмосиликатов. [26]
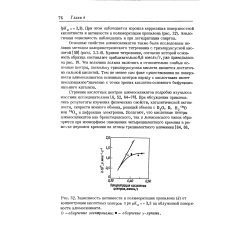 |
Зависимость активности в полимеризации пропилена ( k от концентрации кислотных центров при рКа 3 3 на облученной поверхности алюмосиликата О - облучение электронами. - облучение у-лучами. [27] |
Основные свойства алюмосиликатов также были исследованы недавно методом калориметрического титрования с трихлоруксусной кислотой [50] ( разд. Тем не менее сам факт существования на поверхности алюмосиликатов основных центров наряду с кислотными имеет немаловажное значение с точки зрения кислотно-основного бифункционального катализа. [28]
Исследование с дейтериевой меткой представило прямые доказательства того, что полимерный комплекс является местом протекания реакции изомеризации. В виде импульсов бутен-1 в потоке гелия пропускали над полностью дей-терированной поверхностью алюмосиликата и над алюмосиликатом, имеющим заранее образованный на поверхности полимерный комплекс из молекул пердейтеробутена. Полимерный комплекс на поверхности катализатора был образован в статическом реакторе с использованием смеси цис - и транс-пердейтеробутенов-2. Продукты после каждого импульса анализировались хроматографически и масс-спектрометрически, чтобы определить, переходит ли дейтерий в изомерные бутены. [29]
Изучено ионообменное взаимодействие Na -, Ca -, Ni - и А1 - форм монтмориллонита с растворами бутиламмонийхлорида при различных температурах. Показано, что время установления равновесия зависит от энергии связи неорганических катионов с поверхностью алюмосиликата. Если на Na-форме монтмориллонита равновесие обмена устанавливается за 30 мин. Равновесие обмена на алюминиевой форме наступает только через 10 суток. Показано также, что в случае Na-формы глинистого минерала скорость обмена из разбавленных растворов обусловлена только пленочной кинетикой. В случае солевых форм минералов с многовалентными катионами пленочная кинетика осложнена факторами, обусловленными специфическим поведением частиц в системе глинистый минерал - вода. [30]
Страницы: 1 2 3 4