Поверхность - силикагель
Cтраница 2
На поверхности силикагеля в обычных условиях наблюдается только один тип функциональных групп - силанольные группы. Другая возможная поверхностная структура, состоящая из силок-сановых связей, никогда прямо доказана не была. Это, возможно, обусловлено их химической инертностью. Если гидратированный силикагель нагревать до температур, не превышающих 400 - 500, то образуются так называемые напряженные силоксановые связи, которые легко превращаются обратно в силанольные группы при действии воды. Если силикагель нагревать до более высоких температур, то напряжение снимается и поверхность становится неактивной. Полагают, что это напряжение связано с сильной деформацией 5Ю4 - тетраэдров на поверхности. [16]
 |
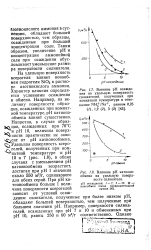
Влияние пористой структуры силикагеля на разделение олиго-фениленов ( фирма Merck 75 - 36. [17] |
Поскольку поверхность силикагелей проявляет слабые кислотные свойства, то соединения с основными свойствами, особенно если элюент полярный, удерживаются сильнее, чем кислые и нейтральные вещества. Продажные силикагели часто нейтрализуют, добавляя к ним основания. [18]
 |
Зависимость величин U трех углеводородов от числа атомов углерода, измеренная при трех различных температурах на широкопористом силикагеле. [19] |
Величины поверхностей силикагелей были рассчитаны также по методу БЭТ из адсорбционных изотерм бутана. [20]
 |
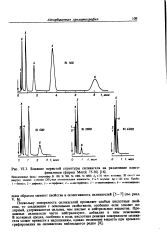
Изотермы сорбции брома на исходном ( / и моди-фициропанном ( вииид-кремнеземв си лика-геле ( 2. [21] |
Модифицирование поверхности силикагеля органическими радикалами с четко выраженными основными или кислотными свойствами приводит к получению специфических адсорбентов и ионообмештиков с ненабухяющим скелетом. [22]
Дегидратация поверхности силикагеля резко снижает адсорбцию веществ, способных к специфическому взаимодействию с гидро-ксильными группами и слабо влияет на неспецифическую адсорбцию, обусловленную вандерваальсовым взаимодействием. Силикагель содержит 99 7 % SiO2 и 0 3, окислов Fe, Al, Ti, Na, Ca и др. Удельная поверхность промышленных силикагелей колеблется в пределах 100 - 1000 м / г ( см. табл. 18, стр. [23]
Дегидратация поверхности силикагеля резко снижает адсорбцию веществ, способных к специфическому взаимодействию с гид-роксильными группами, и слабо влияет на неспецифическую адсорбцию, обусловленную ван-дер-ваальсовым взаимодействием. [24]
 |
Зависимость величин U трех углеводородов от числа атомов углерода, измеренная при трех различных температурах на широкопористом силикагеле. [25] |
Величины поверхностей силикагелей были рассчитаны также по методу БЭТ из адсорбционных изотерм бутана. [26]
Так как поверхность силикагеля покрыта ОН-группами, то можно-было бы ожидать, что спектр ЭПР радикалов - NH2 на нем, так же как в водном растворе аммиака, будет характеризоваться квинтипле-том шириной - 120 гс. Однако спектр - NH2, адсорбированного на поверхности силикагеля. Расщепление между ними равно 26 гс. [27]
Например, поверхности силикагелей, осажденных при рН 7 и 10 и обмененных при рН 10, равны 250 и 60 м2 / г соответственно. [29]
 |
Адсорбенты, выпускаемые для колоночной жидкостной хроматографии. [30] |
Страницы: 1 2 3 4