Поверхность - силикагель
Cтраница 3
Значение рН поверхности силикагелей сильно влияет на удерживание полярных веществ, особенно веществ основного или кислого характера. Для оптимизации селективности разделения необходимо регулировать рН поверхности силикагеля. [31]
 |
Изотермы адсорбции пара бензола при 25 С на силохроме С-120 ( 1, карбосилохро-ме ( 2 и на графитированной термической саже ( 3. [32] |
Нанесение на поверхность силикагеля пироуглерода увеличивает энергию неспецифических дисперсионных взаимодействий. На это указывает более сильное удерживание алканов на карбосили-кагелях по сравнению с силикагелем. [33]
Полярный характер поверхности силикагеля не позволяет использовать его для отбора проб в дождливую погоду, так как вода, сорбируясь на силикагеле, может препятствовать эффективному концентрированию других веществ, а при продолжительной аспирации ( например, при круглосуточном отборе) - вытеснять уже сорбированные соединения. [34]
При насыщении поверхности силикагеля бензонитрильным комплексом хлорида палладия избыток комплекса способствует образованию полидентантных комплексов, обладающих меньшей активностью. [35]
Увеличение размера поверхности силикагелей под действием соляной и азотной, а также слабой серной кислот Шейнфайн [28] объяснила ростом гидрофильно-сти, повышающей степень гидратации первичных частиц и тем самым способствующей их стабилизации. [36]
Уменьшение величины поверхности силикагеля при увеличении содержания катионов ранее было объяснено тем, что замена гидроксильных групп на поверхности частиц золя или геля катионами снижает их гидрофиль-ность, что ведет к потере устойчивости и в итоге к коа-лесценции. Этот процесс обусловлен переносом вещества с выпуклой части поверхности глобулярных частиц в места контакта между ними, возникающие при сближении частиц под действием капиллярных сил при сушке. [37]
Полярный характер поверхности силикагеля не позволяет использовать его для отбора проб в дождливую погоду, так как вода, сорбируясь на силикагеле, может препятствовать эффективному концентрированию других веществ, а при продолжительной аспирации ( например, при круглосуточном отборе) - вытеснять уже сорбированные соединения. [38]
Химическое состояние поверхности силикагеля, обусловливающее его высокую адсорбционную активность по отношению к полярным веществам, сохраняется только при сравнительно низкой температуре ( до 200 С), если десорбция проводится сухим газом. [39]
Полярный характер поверхности силикагеля обусловливает его гидрофильность. Вода, обычно содержащаяся в воздухе в значительных количествах ( 0 015 г / л и выше), значительно снижает адсорбционные возможности сорбента. Можно считать, что 1 г сили - - кагеля почти полностью насыщен парами воды после пропускания 10 - 20 л воздуха. Поглощение паров воды сказывается особенно сильно при улавливании летучих неполярных веществ. В этом случае целесообразно предварительно удалить воду из анализируемого воздуха пропусканием его через слой осушителя, который не сорбирует определяемое вещество, например через диатомитовый носитель, пропитанный растворами хлоридов кальция или лития. [40]
Влияние дегидратации поверхности силикагеля на адсорбцию паров бензола и гексана. [41]
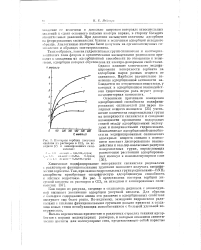 |
Изотермы сорбции уксусной кислоты из растворов в CCU на исходном ( 7 и аминированвых силикагелях. [42] |
Химическое модифицирование поверхности силикагеля радикалами о различными функциональными группами позволяет получать специфические сорбенты. Так, при замене гидроксильных групп радикалами - RNH2 адсорбенты приобретают специфическую адсорбционную способность к кислым веществам. [43]
Десорбцию нитрилов с поверхности силикагеля в пробирку проводят этиловым спиртом, добавляя каждый раз по 0 2 см спирта. Последнюю порцию спирта выдувают резиновой грушей. Затем во все пробирки приливают по 2 0 см3 0 5 н раствора натрия гидроксида и 0 5 см3 насыщенного раствора пикриновой кислоты. Пробирки помещают на водяную баню, нагретую до 80 С, на 30 мин. [44]
Гидроксилыше группы на поверхности силикагеля и кварца определяют их адсорбционные свойства. Поскольку поверхность полнрна, силикагель хорошо поглощает полярные и значительно менее неполярные вещества. Если молекулы адсорбента способны образовывать водородную связь с гидроксилями поверхности, например, вода и спирты, адсорбционные свойства резко зависят от концентрации гидроксилышх групп. Гидроксильные группы являются для целого ряда веществ активными адсорбционными центрами. [45]
Страницы: 1 2 3 4