Поверхность - силикагель
Cтраница 4
Адсорбция молекул на поверхности силикагеля вследствие хотя бы того, что его поверхность покрыта гидроксильными группами, отличается от адсорбции в цеолитах. [46]
Силанольные группы на поверхности силикагеля реагируют как слабые кислоты. Карман [169] обнаружил, что частицы силикагеля приобретают в щелочных растворах отрицательный заряд. [47]
Силанольные группы на поверхности силикагеля можно заместить на различные органические соединения, в частности кремнеор-ганические. На рис. V.1 представлена схема получения химически модифицированного силикагеля. [48]
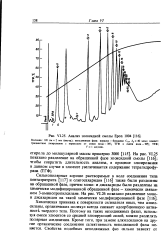 |
Анализ эпоксидной смолы Ероп 1004. [49] |
Химическая прививка к поверхности силикагеля иных, чем алкил-силаны, органических молекул всегда снижает адсорбционную активность твердого тела. [50]
Какие группировки на поверхности частично дегидрокси-лированного силикагеля участвуют в реакции с четыреххлори-стым углеродом. [51]
По мере дегидратации поверхности силикагеля возможность хемо-сорбции воды и метанола растет. [52]
Для химического модифицирования поверхности силикагеля были применены также реакции с гексаметидисилазаном [20] и диметилди-хлорсиланом [21], которые привели к близким результатам. [53]
Обработка тетраборатом калия поверхности силикагеля практически не оказала влияния на величину максимального выхода формальдегида. Несколько снизилась температура, при которой достигается максимум, и уменьшилось содержание СО в конечном газе. [54]
По мере дегидратации поверхности силикагеля ьозможность хемо-сорбции воды и метанола растет. [55]
Адсорбционные же свойства гидроксильной поверхности силикагеля и его Са-замещенных авторы [ ] считают полностью идентичными, с чем, однако, трудно согласиться. [56]
Мы предполагали, что поверхность силикагеля предельно заполнена гидроксильными группами, которые не позволяют адсорбированным молекулам приблизиться к поверхности силикатного скелета. Тогда можно считать, что силовое поле в адсорбированном слое в первом приближении определяется только наличием гидроксильных групп. [57]
Последние частично стабилизируются ка поверхности силикагеля и регистрируются в спектрах ЭПР, Этот процесс изучался нами ранее в 5 - ], Однако процесс фотоактивации, по-видимому, непосредственно не связан со стабилизированными атомами Н, т.к. кинетика их накопления ие соответствует характеру изменения каталитической активности иод действием света. Кроме того, при разогревании образцов атомы Н рекомбинирухя гораздо раньше, чем происходит отжиг активных центров реакции изотопного обмена. [58]
Гайера является распределенный на поверхности силикагеля весьма активный гидроалюмосиликат, имеющий кислые свойства и образовавшийся в результате хемосорбции гидроокиси алюминия гелем кремневой кислоты. Установлено, что кислые свойства глин связаны с наличием в них алюминия. Гидросиликаты одно - и двухвалентных металлов имеют нейтральный или щелочной характер, поэтому они не полимеризуют олефинов. [59]
По существующим взглядам, поверхность силикагеля покрыта гидро-ксильными радикалами, которые в значительной степени обусловливают его адсорбционную способность. Уменьшение гидроксильных групп на поверхности силикагеля может быть достигнуто путем термического воздействия или же заменой их другими радикалами. [60]
Страницы: 1 2 3 4