Корродирующая поверхность - металл
Cтраница 2
При достаточно тонкой дисперсности и равномерном распределении катодов на корродирующей поверхности металла уже при малой общей поверхности катодных участков используются [ see пути для подвода кислорода ( рис. 18) и дальнейшее увеличение числа катодных участков практически не изменяет количества притекающего кислорода и, следовательно, не влияет на коррозионный процесс. Этим можно, в частности, объяснить, что в неподвижных нейтральных электролитах скорость коррозии сталей с различным содержанием углерода не зависит от содержания последнего. [16]
При достаточно тонкой дисперсности и равномерном распределении катодов на корродирующей поверхности металла уже при малой общей поверхности катодных участков используются все пути для подвода кислорода ( рис. 18) и дальнейшее увеличение числа катодных участков практически не изменяет количества притекающего кислорода и, следовательно, не влияет на коррозионный процесс. Этим можно, в частности, объяснить, что в неподвижных нейтральных электролитах скорость коррозии сталей с различным содержанием углерода не зависит от содержания последнего. [17]
Механизм действия анодных ингибиторов основан на пассивации анодных участков корродирующей поверхности металла. Поэтому их называют также пассиваторами. Чаще всего в качестве пассиваторов применяют неорганические окислители, такие как хроматы, нитриты, молибдаты, вольфраматы. [18]
Так, бикарбонат кальция в подщелоченной среде ( у катодных участков корродирующей поверхности металлов) дает нерастворимые соединения СаСО3, осаждающиеся и изолирующие часть поверхности от действия электролита. Этим, в частности, объясняется меньшая скорость коррозии стали в жесткой воде по сравнению с дистиллированной водой. [19]
Цель работы - обнаружить работу гальванических элементов, отводя микротоки с корродирующей поверхности металла, определить направления и величины этих токов, вызванных различными причинами, и исследовать влияние электрохимической гетерогенности поверхности на коррозионную стойкость металла. [20]
 |
Гетерогенная структура сплава. [21] |
В основе первой электрохимической теории коррозии лежало представление об электрохимической неоднородности корродирующей поверхности металла. Металлы состоят из беспорядочно ориентированных кристаллитов ( или зерен) с хорошо выраженной границей. Примеси при затвердевании металлов концентрируются на границах зерен. Еще более неоднородна поверхность технических металлов и их сплавов. [22]
 |
Зависимость скорости коррозии стали в нейтральных водных растворах от концентрации NaoSiCb. [23] |
Известны также анодные замедлители коррозии вторичного действия, образующие на анодных участках корродирующей поверхности металла нерастворимые продукты коррозии вследствие взаимодействия ионов растворяющегося металла с замедлителем. [24]
В большинстве случаев протекание электрохимической коррозии характеризуется локализацией анодного и катодного процессов на различных участках корродирующей поверхности металла, что приводит к неравномерному или местному коррозионному разрушению металлической поверхности. На процессы электрохимической коррозии металлов существенно влияют как внутренние, так и внешние факторы. [25]
Важно отметить, что образование осадка Fe ( OH) 2 обычно происходит не непосредственно на корродирующей поверхности металла, а в толще раствора, где встречаются диффундирующие продукты катодной и анодной реакции коррозионного процесса. Полученный при этом рыхлый осадок не изолирует металл от доступа электролита и не может поэтому прекращать коррозию металла. Только в тех случаях, когда катод и анод находятся в непосредственном контакте, можно ожидать образования на корродирующей поверхности пленки гидроокиси, способной защищать металл от коррозии. [26]
 |
K. wd - 1 анодной пассивности. [27] |
Это происходит потому, что в условиях перемешивания практически отсутствуют диффузионные ограничения, и Ог беспрепятственно поступает к корродирующей поверхности металла. Беспрепятственно также осуществляется н отвод продуктов коррозии. [28]
Это происходит потому, что в условиях перемешивания практически отсутствуют диффузионные ограничения, и О2 беспрепятственно поступает к корродирующей поверхности металла. Беспрепятственно также осуществляется и отвод продуктов коррозии. [29]
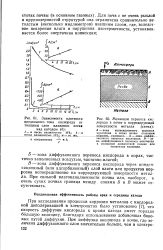 |
Зависимость плотности предельного тока кислорода от толщины слоя влажного песка над катодом ( h.| Механизм переноса кислорода в почве к корродирующей поверхности металла ( схема. [30] |
Страницы: 1 2 3 4 5