Повышение - концентрация - электролит
Cтраница 3
Количество поглощенного водорода снижается с увеличением температуры, повышением концентрации электролита и понижением катодной плотности тока. [31]
Начальную стадию коагуляции, когда ее скорость увеличивается пропорционально повышению концентрации электролита, называют медленной коагуляцией. В дальнейшем процесс агрегации достигает максимальной скорости, не зависящей от концентрации добавленного электролита. Эту стадию называют быстрой коагуляцией. Коагуляция сопровождается помутнением золя, затем дисперсная фаза выпадает в осадок ( коагулят) или образуется гель. [32]
Оказалось, что уменьшение равновесной толщины пленок пены с повышением концентрации электролита в присутствии олеата натрия очень хорошо соответствует теоретически вычисленной зависимости. [33]
Вытеснение маслорастворимых ПАВ из адсорбционного слоя часто достигают при повышении концентрации электролита. Увеличение содержания ионов приводит к дегидратации полярных групп молекул ПАВ и вызывает снижение энергии адсорбции. [34]
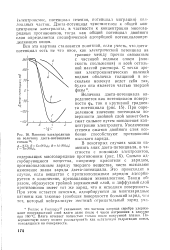 |
Влияние электролитов бенно способствуют противоионы на величину дзета-потенциала высокого заряда. [35] |
При определенном значении потенциала поверхности двойной слой может быть сжат сильнее путем повышения концентрации электролита. [36]
По мере испарения электролита в ванну следует добавлять чистую воду, так как повышение концентрации электролита приводит к ухудшению качества окраски. Если окраска получилась неудачной, пленку можно легко снять. Детали, окрашенные этим способом, промывают водой, сушат и покрывают тонкой пленкой бесцветного лака. [37]
При воздействии нелетучих электролитов на гидрофобные полимеры через пленку проникает лишь воде и, поскольку при повышении концентрации электролита активность воды падает, адгезионная про кость покрытий снижается менее интенсивно. [38]
Результаты опытов, в которых изучалось влияние избытка электролита на сорбцию противоионов, показали, что при повышении концентрации электролита сорбция катионов увеличивается. Это указывает на-т ОТчто при - введении электролитов в количестве, превышающем порог коагуляции, происходит дополнительная адсорбция потенциалопределяющих ионов, всегда присутствующих в ин-термицеллярной жидкости. В связи с этим возрастает плотность заряда на поверхности дисперсной фазы и соответственно увеличивается ее сорбционная емкость. [39]
Результаты опытов, в которых изучалось влияние избытка электролита на сорбцию противоионов, показали, что при повышении концентрации электролита сорбция катионов увеличивается. Это указывает на то, что при введении электролитов в количестве, превышающем порог коагуляции, происходит дополнительная адсорбция потенциалопределяющих ионов, всегда присутствующих в ин-термицеллярной жидкости. В связи с этим возрастает плотность заряда на поверхности дисперсной фазы и соответственно увеличивается ее сорбционная емкость. [40]
Порядок полученных значений линейного натяжения, равно как и то, что оно меняет свой знак под влиянием повышения концентрации электролита, не вызывают сомнений. Последнее противоречит теоретическому выводу де Фейтера и Врея [17], что пленки всегда должны иметь отрицательное линейное натяжение по линии перехода к большой жидкости. [41]
Так, К. П. Мищенко на обширном экспериментальном материале показал для разных групп электролитов, как меняются свойства воды по мере повышения концентрации электролита в растворе при разных температурах. Он показал, что, в отличие от других растворителей, в которых повышение температуры всегда ослабляет сольватацию ионов, в воде уменьшение связей между молекулами, происходящее с повышением температуры ( см. § 73), в какой-то степени облегчает гидратацию ионов, поэтому повышение температуры может меньше ослаблять гидратацию ионов или даже сопровождаться повышением гидратации их. [42]
Таким образом, при постоянной концентрации солянокислой соли хитозана в водных растворах эффективная константа скорости реакции озона с хитозаном уменьшается с повышением концентрации электролита в реакционной среде, что связано с влиянием ионной силы раствора на конформацию макромолекул полисахарида. [43]
Таким образом, при постоянной концентрации солянокислой соли хитозана в водных растворах эффективная константа скорости реакции озона с хитозаном уменьшается с повышением концентрации электролита в реакционной среде, что связано с влиянием ионной силы раствора на конформацию макромолекул полисахарида. [44]
Количество образующихся и переходящих в газ водяных паров увеличивается с повышением температуры в ванне и уменьшается при повышении давления электролиза и повышении концентрации электролита. [45]
Страницы: 1 2 3 4