Повышение - концентрация - электролит
Cтраница 4
Результаты исследования устойчивости дисперсии алмаза в растворах LiCl ( 10 2 - 5 - Ю 1 моль / л) при рН, равных 2, 3 и 6, и температуре опыта 20, 40 и 50 С [25] показали, что с ростом температуры и повышением концентрации электролита устойчивость системы также уменьшается. [46]
Результаты исследования устойчивости дисперсии алмаза в растворах LiCl ( 10 - 2 - 5 - Ю 1 моль / л) при рН, равных 2, 3 и 6, и температуре опыта 20, 40 и 50 С [25] показали, что с ростом температуры и повышением концентрации электролита устойчивость системы также уменьшается. [47]
Теории, объясняющие коагуляцию лиофобных золей растворами электролитов, можно в основном разделить на две группы: теории адсорбционные, исходящие из представлений, что коагуляция обусловливается адсорбцией коллоидными частицами ионов прибавленного электролита, и электростатические, связывающие коагуляцию с изменением размеров и свойств двойного электрического слоя вокруг частиц при повышении концентрации электролита в системе. [48]
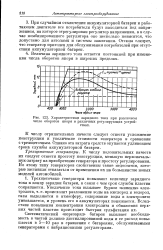 |
Характеристики зарядного тока при различном числе оборотов якоря и различных регулирующих устройствах. [49] |
Трехщеточные генераторы повышают величину зарядного тока к концу зарядки батареи, в связи с чем срок службы пластин сокращается. Вследствие повышения концентрации электролита и обнажения верхних частей пластин происходит быстрая сульфатация их. [50]
Строго говоря, выражение (4.12) справедливо лишь для бесконечно разбавленных растворов. С повышением концентрации электролита начинают проявляться различия между процессами диффузии и миграции под действием внешнего электрического поля. [51]
При малой концентрации все электролиты в водном растворе полностью распадаются на ионы. С повышением концентрации электролита его способность распадаться на ионы уменьшается. [52]
Эквивалентная электропроводность ( подвижность) уменьшается с повышением концентрации раствора. При повышении концентрации электролита увеличивается ионная сила и скорость движения ионов уменьшается за счет межионных взаимодействий. [53]
На рис. 17 представлена группа кривых ( по вычислениям Фервея и Овербека), показывающих зависимость потенциальной энергии взаимодействия двух коллоидных частиц от расстояния между ними; взяты наиболее вероятные значения потенциала поверхности и ван-дер-ваальсового притяжения. При повышении концентрации электролита, что соответствует увеличению значений к, отталкивание постепенно переходит в притяжение при достаточно малых расстояниях между частицами. [54]
Страницы: 1 2 3 4