Повышение - адсорбция
Cтраница 3
Как правило, соединения ароматического ряда той же химической природы и с одинаковым числом атомов углерода адсорбируются больше, чем алифатические. Введение гидроксильной группы, а также сульфогруппы уменьшает адсорбцию. Карбоксильная группа и галогены в алифатических соединениях способствуют повышению адсорбции. При адсорбции молекулы ПАВ в пограничном слое ориентируются таким образом, что свободная энергия поверхностного слоя снижается. Очевидно, что адсорбция при этом должна зависеть не только от природы адсорбента, но и от природы растворителя и адсорбируемого вещества. Согласно правилу уравнивания полярностей ПАВ должны адсорбироваться в поверхности раздела твердое тело - жидкость тем больше, чем больше между ними разность полярностей, иначе говоря, чем больше будет оказываемое обеими фазами ориентирующее влияние на адсорбируемые молекулы. Ориентация полярных молекул в поверхносиГраздела твердое тело - жидкость происходит таким образом, что своею полярной частью молекулы должны быть обращены к поверхности адсорбента, если она гидрофильна, углеводородной же частью - в сторону неполярного или малополярного растворителя и наоборот - для системы гидрофобный адсорбент - полярный растворитель. [31]
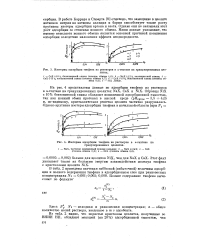 |
Изотермы адсорбции тиофена из растворов в к-гептане на гранулированных цеолитах.| Изотермы адсорбции тиофена из растворов в и-гептане гранулированных цеолитах. [32] |
В работе Баррера и Стюарта [8] отмечено, что замещение в цеолите катионов натрия на катионы кальция и бария способствует также росту крутизны изотерм адсорбции аргона и азота. Наши данные указывают, что именно неполнота ионного обмена является основной причиной повышения адсорбции вследствие наложения эффекта неоднородности. [33]
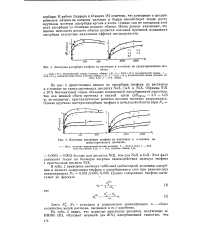 |
Изотермы адсорбции тиофена из растворов в w - гептане на гранулированных цеолитах.| Изотермы адсорбции тиофена из растворов в к-гептане на гранулированных цеолитах. [34] |
В работе Баррера и Стюарта [8] отмечено, что замещение в цеолите катионов натрия на катионы кальция и бария способствует также росту крутизны изотерм адсорбции аргона и азота. Наши данные указывают, что именно неполнота ионного обмена является основной причиной повышения адсорбции вследствие, наложения эффекта неоднородности. [35]
Адсорбция органических веществ из раствора равномерно возрастает по мере увеличения длины углеводородной цепи. Это справедливо для гладкой поверхности твердого тела. Для пористых тел, наоборот, с увеличением числа атомов углерода в молекуле наблюдается не повышение адсорбции, а понижение ее. [36]
Из данных табл. 29 следует, что удельная адсорбция эмульгатора ЭС-2 ( без растворителя) на исследованных минералах происходит во времени. Практически предельная адсорбция наступает в течение 1 ч, что соизмеримо со временем утяжеления обратных эмульсий в производственных условиях. Увеличение температуры опытов с 20 до 50 С на адсорбции практически не сказывается, а ее рост до 70 С приводит к повышению адсорбции ЭС-2 на бентонитовой глине, незначительному возрастанию на песке и снижению, примерно в два раза, на меле и барите. [37]
Подобно этому газ 1 уменьшает адсорбцию газа 2 соответственно его парциальному давлению и адсорбционному коэффициенту рг и &. Из уравнений ( 5) и ( 6) следует, что один газ всегда уменьшает адсорбцию другого. Повышение адсорбции другого газа не может быть объяснено на основе теории Лэнгмюра. [38]
Другими словами, в этом случае адсорбция под влиянием другого газа скорее повышается, чем уменьшается. Причиной этого, без сомнения, является то, что между адсорбированными молекулами углекислого газа и окиси углерода возникают силы взаимного притяжения, повышающие теплоту адсорбции углекислого газа ( гл. Адсорбция углекислого газа увеличивается подобным образом при наличии высоких парциальных давлений окиси углерода. Другие примеры повышения адсорбции мы обсудим позднее. [39]
Пыли исследованы нитрат и сульфат аммония - соли, анионы которых занимают весьма различное положение в лиотропном ряду, а также хлорид двухвалентного катиона кальция. С качественной точки зрения во всех случаях независимо от степени оксиэтилирования эфира наблюдались одинаковые закономерности ( см. рис. 1 - 4): в присутствии электролитов величина адсорбции ПАВ в большей или меньшей мере всегда возрастала. Иногда, правда, повышение адсорбции столь невелико, что па рисунках оно незаметно. [40]
Помимо этого, изменения удельной активности, наблюдавшиеся Кейер и др. [95], оказались очень значительны. Возможно, что наблюдаемую при этих температурах пониженную активность закиси никеля, содержащей литий, следует объяснить исходя из того, что такой окисел адсорбирует те или иные частицы, участвующие в реакции, гораздо интенсивнее, чем чистая закись. Кейер и Куцева [99] сообщили, что введение добавок лития ( при условии не слишком больших количеств) способствует повышению адсорбции кислорода и углекислого газа при комнатной температуре. [41]
Помимо этого, изменения удельной активности, наблюдавшиеся Кейер и др. [95], оказались очень значительны. Возможно, что наблюдаемую при этих температурах пониженную активность закиси никеля, содержащей литий, следует объяснить исходя из того, что такой окисел адсорбирует те или иные частицы, участвующие в реакции, гораздо интенсивнее, чем чистая закись. Кейер и Куцева [99] сообщили, что введение добавок лития ( при условии не слишком, больших количеств) способствует повышению адсорбции кислорода и углекислого газа при комнатной температуре. [42]
На рис. 1.7 и 1.8 представлены изотермы адсорбции и доли связанных сегментов при различных соотношениях адсорбент-раствор. Существенным является то, что сразу после адсорбции в растворе не обнаруживаются агрегаты; они восстанавливаются в растворе в результате установления нового равновесия в системе агрегат - макромолекула. Такая зависимость объясняется тем, что при адсорбции на поверхность прежде всего переходят агрегаты, а затем изолированные макромолекулы. Так как число агрегатов значительно меньше числа макромолекул в растворе, то при условии полной адсорбции агрегатов ( а это наблюдалось экспериментально), увеличение содержания адсорбента способствует повышению адсорбции неагрегированных молекул и снижению общей величины адсорбции. [43]
Газ 2 уменьшает адсорбцию газа 1 тем больше, чем больше рг и Ь2 т - е - его парциальное давление и коэффициент адсорбции. Подобно этому газ 1 уменьшает адсорбцию газа 2 соответственно его парциальному давлению и адсорбционному коэффициенту рг и Ьг. Из уравнений ( 5) и ( 6) следует, что один газ всегда уменьшает адсорбцию другого. Повышение адсорбции другого газа не может быть объяснено на основе теории Лэнгмюра. [44]
Другими словами, в этом случае адсорбция под влиянием другого газа скорее повышается, чем уменьшается. Причиной этого, без сомнения, является то, что между адсорбированными молекулами углекислого газа и окиси углерода возникают силы взаимного притяжения, повышающие теплоту адсорбции углекислого газа ( гл. Адсорбция углекислого газа увеличивается подобным образом при наличии высоких парциальных давлений окиси углерода. Другие примеры повышения адсорбции мы обсудим позднее. [45]
Страницы: 1 2 3 4