Подвижность - ион - водород
Cтраница 1
Подвижность ионов водорода равна 313 кулон см / сек, а подвижность ионов F -, N03 -, Уг SOn изменяется в пределах от 46 6 до 67 кулон см / сек. [1]
Подвижность ионов водорода в Pd быстро растет с температурой и во много раз превышает таковую для углерода в железе. Высокие значения ее ( 1 5 - 10 - 4 см2 сект1 в-1 при 182 С) в электрическом поле находятся в соответствии с большой величиной коэффициента диффузии водорода ( 1 5 10 - 5 см2 - сект1 при 180 С в Pd) и с весьма малыми размерами его катионов. [2]
 |
Электрометрическое титрование кислот щелочью. [3] |
Подвижность ионов водорода значительно выше подвижности ионов натрия, поэтому электропроводность раствора падает. [4]
Подвижность ионов водорода почта в 5 раз выше подвижности ионов хлорида, поэтому со стороны более концентрированного раствора граница заряжена отрицательно. [5]
Для льда подвижность ионов водорода оказывается на два порядка выше, чем в воде, и превышает подвижность других катионов во льду более чем на восемь порядков. Столь высокая подвижность обусловлена благоприятной для перескока протона упорядоченностью структуры льда, а также тем, что концентрация ионов водорода во льду существенно меньше, чем в воде, и молекулы Н2О успевают реориентировать-ся в период между двумя последовательными перескоками протона. В таких условиях весь процесс лимитируется стадией протонного тун-нелирования. [6]
Для льда подвижность ионов водорода оказывается на два порядка выше, чем в воде, и превышает подвижность других катионов во льду более чем на восемь порядков. Столь высокая подвижность обусловлена благоприятной для перескока протона упорядоченностью структуры льда, а также тем, что концентрация ионов водорода во льду существенно меньше, чем в воде, и молекулы НаО успевают реориентироваться в период между двумя последовательными перескоками протона. В таких условиях весь процесс лимитируется стадией протонного туннелирования. [7]
Резкое отличие подвижности иона водорода и гидроксид-иона от подвижности других ионов используется в методе кондук-тометрического титрования. Сущность метода заключается в том, что во время титрования периодически измеряют закономерно изменяющуюся электропроводность раствора и строят кривую в координатах электропроводность - объем раствора, пошедшего на титрование. Точку эквивалентности определяют по резкому изменению хода кривой. Метод применяют при объемном анализе сильно окрашенных или мутных растворов, в которых не могут быть использованы окрашенные индикаторы. Роль индикатора здесь играет электропроводность. [8]
 |
Определение чисел переноса i методом движущейся границы. [9] |
Как указывалось, подвижности ионов водорода и гидроксила в водных растворах аномально велики по сравнению с подвижностями других ионов. [10]
Поэтому изменение отношения подвижностей ионов водорода и натрия не может влиять на степень регенерации ионита, а наблюдаемое увеличение степени регенерации слабоэлектролитных ионитов при повышении температуры можно, вероятно, объяснить только фактором возрастания степени гидролиза этих солей. [11]
Кроме перечисленных факторов, изменение подвижности иона водорода, очевидно, связано с прототропным механизмом проводимости ( разд. [12]
В солеобразующей оксимной группе - N-ОН подвижность иона водорода зависит от строения молекулы оксима. Это позволяет выделять соединения никеля при определенных значениях рН в растворе, используя различные оксимы. С, представляет собой коричневый кристаллический порошок, легко растворимый в горячем спирте, эфире, уксусной кислоте, бензоле, сероуглероде и мало растворимый в воде. [13]
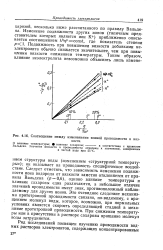 |
Соотношение между изменениями ионной проводимости и вязкости. [14] |
Следует отметить, что зависимость изменения подвижности иона водорода от вязкости заметно отклоняется от правила Вальдена ( / 7 - 0 6), однако влияние температуры и влияние сахарозы едва различаются, а небольшое отличие значений проводимости имеет знак, противоположный наблюдаемому для других ионов. Это очевидное следствие механизма прототропной проводимости связано, по-видимому, с вращением молекул воды, которое, возможно, при нормальных условиях является скорость определяющей стадией в механизме прототропной проводимости. При снижении температуры или в присутствии в растворе сахарозы вращение молекул воды затрудняется. [15]
Страницы: 1 2 3 4