Циклический полиэфир
Cтраница 1
Циклические полиэфиры с числом атомов в кольце больше пяти или шести редко образуются непосредственно, но могут получаться при энергичной обработке полиэфиров. Это, очевидно, происходит вследствие пространственной конфигурации; модели показывают, что вероятность такого сбли-я ения активных конечных групп, чтобы стала возможной реакция, почти ничтожна, если они разделены более чем четырьмя атомами. [1]
Циклические полиэфиры обладают способностью узнавать неорганические ионы: [18] - краун-6 узнает ион калия, [58] - краун-5 узнает ион натрия, а [12] - краун-4 избирательно включает во внутреннюю полость только ион лития. [2]
Циклические полиэфиры приводят к резкому увеличению скорости в растворителях, подобных диоксану [516], где эффект связан, вероятно, с M Y - - ( М СРЮ Т ( разд. [3]
Циклические полиэфиры и соответствующие азотсодержащие соединения ( разд. Образование комплексов Са24 - с ЭДТА4 - и полифосфатами имеет значение не только как способ удаления ионов Са2 из воды, но также для аналитического количественного определения Са2 объемным методом. [4]
Молекулы циклических полиэфиров содержат кольца из атомов кислорода, энергетически способные выполнять роль сольватной оболочки вокруг катиона. Таким образом, происходит внедрение катиона в органическую фаз у. При этом образуются подвижные заряженные комплексы, обеспечивающие ка-тионную проводимость таких сред. Среди них наиболее известен К - селективный электрод с жидкой мембраной - раствором ва-линомииина в органическом растворителе. [5]
Мицеллы, циклические полиэфиры, криптаты и аналогичные молекулярные катализаторы уже применяются для ускорения многих органических реакций, особенно в тонких органических синтезах. Однако возможности таких гомогенных катализаторов в настоящее время только начинают осознаваться. То же относится к применению ферментов для осуществления ряда ключевых процессов органического синтеза. Однако критическое рассмотрение этого обширного материала выходит за рамки данной книги. [6]
Крауны представляют собой простые циклические полиэфиры, со - держащие от 9 до 60 атомов в кольце, в том числе от 3 до 20 атомов кислорода; многие из них при комнатной температуре являются твердыми веществами и далеко не всегда используются как растворители. Некоторые крауны образуют весьма стабильные комплексы с рядом катионов металлов и катионом аммония. В какой-то мере подобными свойствами обладают некоторые бициклические диамины, содержащие оксиметиленовые мостики ( атомы азота расположены в голове мостиковой связи); эти соединения способны капсулировать катионы металлов с образованием криптатов. В обзоре [16] обсуждается способность простых циклических полиэфиров, политио-эфиров, полиаминов и подобных соединений связывать ионы металлов. [7]
Комплексы между циклическими полиэфирами и ионами с одинаковыми зарядами и не сильно отличающимися диаметрами могут сильно различаться по их относительной стабильности; различие в константах стабильности между Са2 и РЬ2 при образовании комплекса с дициклогексил-18 - краун-6 составляет около 105, комплекс с последним ионом является более прочным. Такое селективное различие может иметь определенную ценность с точки зрения токсичности свинца в некоторых биологических системах. При переходе от полярных к менее полярным растворителям ожидается рост стабильности комплексов. Для комплексов с дицикло-гексил-18 - краун-6 ( 109) константы стабильности в случае ионов К и Na при переходе от воды к метанолу повышаются примерно в 104 и в 103 раз соответственно. [8]
Самым замечательным свойством циклических полиэфиров является их способность образовывать с солями металлов комплексы, растворимые в органических растворителях. Эти комплексы проявляют повышенную реакционную способность. Активность таких растворов комплекса, вероятно, обусловлена присутствием несольватнрованных ионов гидро-ксила, у которых реакционная способность гораздо выше, чем у гидроксильиых ионов, сольватированных, как обычно. Ниже приведен еще более эффектный пример использования таких комплексов. [9]
Самым замечательным свойством циклических полиэфиров является их способность образовывать с солями металлов комплексы, растворимые в органических растворителях. Эти комплексы проявляют повышенную реакционную способность. Активность таких растворов комплекса, вероятно, обусловлена присутствием несольватнрованных ионов гидро-ксила, у которых реакционная способность гораздо выше, чем у гидроксильиых ионов, сольватированных, как обычно. Ниже приведен еще более эффектный пример использования таких комплексов. [10]
Здесь речь идет о циклических полиэфирах 17 - краун-эфирах, открытых Педерсеном [ 2с ] в 1960 - х годах ( см. разд. [11]
Здесь речь идет о циклических полиэфирах 17 - краун-эфирах, открытых Педерсеном [ 2с ] в 1960 - х годах ( см. разд. Поэтому комплексы типа 18 уже достаточно хорошо растворимы в органических растворителях, в чем легко убедиться с помощью простого эксперимента: если взять двухфазную систему ярко-окрашенный водный раствор перманганата калия - бесцветный бензол и добавить в нее небольшое количество краун-эфира 17, то бензольный слой немедленно окрашивается в интенсивный малиновый цвет. [12]
О) проникает в дырку циклического полиэфира. [13]
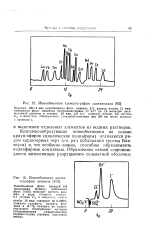 |
Ионообменная хроматография лантаноидов.| Ионообменная хроматография анионов. [14] |
Комплексообразующие ионообменники на основе краун-эфиров ( циклические полиэфиры) отличаются рядом характерных черт ( см. ряд публикаций группы Бла-зиуса) и, что особенно важно, способны образовывать полиэфирные комплексы. [15]
Страницы: 1 2 3 4