Закономерность - подбор - катализатор
Cтраница 4
О механизме разложения спиртов неоднократно говорилось в I части. Перечислим основные выводы по закономерностям подбора катализаторов для разложения спиртов, вытекающие из различных теорий катализа. [46]
В общем, можно сказать, что закономерности подбора катализаторов разложения изопропилового спирта подтверждаются и для этилового спирта. Как и для цзо - С3Н7ОН ( рис. 37), глубокий минимум активности приходится на V205, а максимум на NiO. Сохраняются и другие закономерности. В обоих случаях значительной каталитической активностью обладают щелочноземельные окислы. Для более детального корреляционного анализа, аналогичного проведенному для мзо - С3Н7ОН, данных явно недостаточно. [47]
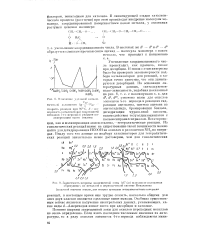 |
Изменение удельной катали.| Зависимость ширины запрещенной зоны Л U ( ав окислов от положения образующих их металлов в периодической системе Менделеева. [48] |
Уменьшение координационного числа происходит, как правило, также при десорбции. В связи с этим интересно было бы проверить закономерности подбора катализаторов для реакций, о которых точно известно, что они лимитируются десорбцией. [49]
За исключением дегидратации спиртов и кислот, а также, возможно, галогенирования бензола и толуола, до сих пор нами рассматривались реакции окислительно-восстановительного или гете-ролитического типа. Значительно меньше надежных данных имеется в литературе по закономерностям подбора катализаторов для реакций кислотно-основного или гетеролитического типа, к рассмотрению которых мы теперь переходим. [50]
Вследствие своей простоты иногда они применяются в качестве модельных реакций для изучения закономерностей подбора катализаторов. [51]
Ноллер и Остермайер [326, 327] исследовали дегидрохлориро-ванве алкилхлоридов: С2Н5С1, С3Н7С1, изо - С3Н7С1, С4Н9С1, втор - С4Н9С1, mpem - CJlgCl и хлорциклогексана на ряде катализаторов: хлоридах щелочных металлов, окислах, карбидах и нитридах Ti, V, Nb, Та, Сг. Несмотря на малую достоверность этих результатов отсутствие измерений поверхности, сведений о режиме реакции, малая величина изученного температурного интервала измерений - 20 - 40 С), авторы делают ряд выводов о механизме реакции и закономерностях подбора катализаторов. [52]
Характерными катализаторами первого типа, как было показано, являются полупроводники, второго - кислоты и основания. Некоторые реакции ( например, разложение спиртов и кислот, полимеризация) могут протекать и по электронному, и по кислотно-основному механизму. Соответственно, закономерности подбора катализаторов усложняются. [53]
В работе [10] предложен механизм реакции ( 1П) [ с адсорбцией молекул спирта и акролеина на соседних атомах металла. Этот исходный принцип, по-видимому, правилен. Детальная схема реакции, на основании полученных выше закономерностей подбора катализаторов и спектральных данных, может быть написана по-другому. [54]
Страницы: 1 2 3 4