Положение - нитрогруппа
Cтраница 2
В какой-то мере, возможно, идет образование изомеров ( положение нитрогруппы в ароматическом ядре), однако они не были выделены, так как, вероятно, их количество невелико. [16]
По женевской номенклатуре названия нитроеоединений строятся так же, но положение нитрогруппы обозначается не греческой буквой, а цифрой, например 1-нитропропан, 2-нитропропан. [17]
Изложенное показывает, что из-за способности а-комплексов к изомеризации, положение нитрогруппы в продуктах нитров ания не всегда соответствует месту первичной атаки катиона нитрония. Таким образом, кинетический контроль реакции нитрования не является абсолютным. [18]
Изложенное показывает, что из-за способности а-комплексов к изомеризации, положение нитрогруппы в продуктах нитрования не всегда соответствует месту первичной атаки катиона нитрония. Таким образом, кинетический контроль реакции нитрования не является абсолютным. [19]
По женевской номенклатуре, названия нитросоединений строятся так же, но положение нитрогруппы обозначается не греческой буквой, а цифрой: 1-нитропропан, 2-нитропропан. [20]
Второй реагент превращает кумарои в смесь 2-питрокумароиа и цуо-мерного соединения с невыясненным положением нитрогруппы. [21]
Для защиты меди нитроо ензО атами, очевидно, важно не столько положение нитрогруппы, сколько число таких групп в соединении. [22]
Не все нитросоединения были выделены в чистом состоянии, не было окончательно установлено положение нитрогруппы в молекуле углеводорода. [23]
Таким образом, ясно видно, что заместители оказывают очень большое влияние на положение вступающей нитрогруппы. [24]
Сопоставление данного случая с камфаном и фенханом позволяет с большой вероятностью еще ближе определить положение нитрогруппы в продукте нитрования р-метилкамфенилана. [25]
Известны шесть изомеров тринитротолуола, имеющих общую формулу СбН2 ( МО2) зСНз, но отличающихся положением нитрогрупп в бензольном ядре, а вследствие этого и физико-химическими свойствами. Применяемый в практике тротил состоит в основном из симметричного ( 2 4 6 -), или а-изомера тринитротолуола. [26]
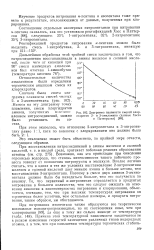 |
Диаграмма плавкости смесей хлор-гидратов 2 - и 3-амиламина ( данные Хэсса и Паттерсона. [27] |
Возможно, как это происходит при окислении перекисью водорода, что степень интенсивности такого побочного процесса зависит от положения нитрогруппы в молекуле. Вполне логично считать, что в одних и тех же условиях восстановление 2-нитропентана железом и соляной кислотой дает меньше амина и больше кетона, чем восстановление 3-нитропентана. Поэтому в смеси двух аминов 3-аминопентана должно было бы находиться больше, чем это получается по анализу. То, что первичный н-нитропентан определяется в продуктах нитрования в большем количестве, чем это следует ожидать на основании аналогии в закономерностях нитрования и хлорирования, объясняется, очевидно, тем, что при высоких температурах нитрования он термически более устойчив, чем остальные изомеры, и продукты нитрования, таким образом, им обогащаются. [28]
При введении заместителей в обе части молекулы гидразона решающим фактором в проявлении как индикаторных, так и общеаналитических свойств оказывается положение нитрогрупп в молекуле исходного фенилгидразина. Заместители в молекуле исходного карбонилсодержащего соединения оказывают меньшее влияние. [29]
Названия нитросоединений производят из названий соответствующих ароматических углеводородов, добавляя к ним приставку нитро -; если требуется, указывают число и положение нитрогрупп. [30]
Страницы: 1 2 3 4