Положение - таутомерное равновесие
Cтраница 1
Положение таутомерного равновесия в известной степени зависит от природы растворителя и концентрации вещества: содержание енола увеличивается в малополярных растворителях ( сероуглерод, гексан) и при разбавлении. Более важными являются структурные особенности. Ацетон по существу содержит только кето-форму, в р-кетоэфирах содержится больше енольной формы, чем в простых кетонах, а высокое содержание енола в 1 3-дикетонах ( ацетилацетоне и бензоилацетоне) свидетельствует о том, что активация двумя карбонильными группами протекает значительно более эффективно, чем активация при сочетании кето - и эфирной групп. Сопряженная с двойной связью енола фенильная группа способствует енолизации. [1]
Положение таутомерного равновесия зависит от ряда факторов и, в частности, от соотношения кислотностей таутомеров. Оно смещено в сторону менее диссоциированного таутомера, обладающего меньшим запасом свободной энергии. Следовательно, если / т1, то равновесие смещено в сторону кетонной формы и енольная форма является более сильной кислотой. Если / Сг 1, то преобладает енольная форма и кетонная форма - более сильная кислота. Поэтому распространенное представление о большей кислотности ено-лов ошибочно. [2]
Положение таутомерного равновесия зависит от ряда факторов, и в частности от соотношения кислотностей таутомеров. Оно смещено в сторону менее диссоциированного таутомера, обладающего меньшим запасом свободной энергии. Следовательно, если / Ст 1, то равновесие смещено в сторону кетонной формы и енольная форма является более сильной кислотой. Если 1 ( Т 1, то преобладает енольная форма и кетонная форма - более сильная кислота. Поэтому распространенное представление о большей кислотности ено-лов ошибочно. [3]
Положение таутомерного равновесия зависит от влияния заместителей в ароматических кольцах. Например, в приведенном случае преобладает второй таутомер. [4]
Положение таутомерного равновесия зависит от применяемого растворителя. [5]
Положение таутомерного равновесия в случае замещения аминопи-ридинов существенно зависит от заместителя в NHX. [6]
Положение таутомерного равновесия зависит от применяемого растворителя. [7]
Положение таутомерного равновесия в случае замещения аминопири-динов существенно зависит от природы радикала R. Например, в ряду арилсульфаминопиридинов как показали М. И. Кабачник, Т. А. Мастрю-кова, Ю. Н. Шейнкер и И. К. Кузнецова, в зависимости от характера радикала R существенно изменяются кислотные свойства форм и меняется положение равновесия. [8]
 |
Константы равновесия кето-енолов. [9] |
Для определения положения таутомерного равновесия применяют химич. Первые пригодны лишь в том случае, если под влиянием добавляемого реагента не происходит смещение равновесия, и реакция с этим реагентом протекает быстрее, чем само таутомерное превращение. Для обнаружения ifuc - енолышх форм применяется качественная реакция с хлорным железом, а также образование медного внутрикомплеке-ного соединения с ацетатом меди. [10]
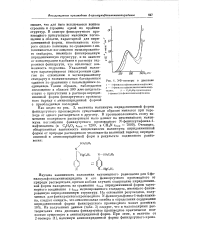 |
УФ-спектры в диоксане. [11] |
Изучена зависимость положения таутомерного равновесия для 4-фе-нилсульфониламинопиридина и его фенилртутного производного от природы растворителя, причем в обоих случаях содержание пиридониминной формы находилось из сравнения етах пиридониминной формы тауто-мерного соединения с етах метилированного стандарта, имеющего фиксированную пиридониминную структуру. Из полученных данных ( табл. 3) следует, что в малополярных растворителях типа диоксана фенилртутное производное практически полностью существует в аминопиридинной форме. [12]
Влияние растворителей на положение таутомерного равновесия, во многих случаях определяющееся водородными связями, широко известно и здесь рассматриваться не будет. [13]
Влияние растворителей на положение таутомерного равновесия, во многих случаях определяющееся водородными связями, широко известно и здесь рассматриваться не будет. [14]
 |
График зависимости 1 от о. [15] |
Страницы: 1 2 3 4