Положение - таутомерное равновесие
Cтраница 3
Для 1-фенил - 3-метил - 4-фенилазо - 5-пиразолона, 2-фе-нилазорезорцина, 2 4-бис ( фенилазо) - 1-нафтола, фенилгидразона антрахинона, 1-фенилазо - 4-нафтола [32], десяти этиловых эфиров napa - замещенных фенилгидразиноцианоацетилкарбаминовых кислот и арилгидразино-2 - цианометилбензимидазола [33] положение таутомерного равновесия также было определено путем исследования методом ПМР меченых ( 15N) соединений. [31]
Таутомерное равновесие характеризуется его положением и скоростью установления. И положение таутомерного равновесия, и скорость его установления весьма различны. [32]
Это предвидение основывалось на сопоставлении диалкиланилидофосфитов с диалкилфосфитами, положение равновесия которых хорошо известно. Действительно известно, что положение таутомерного равновесия всегда смещено в сторону формы, обладающей меньшими кислотными свойствами. [33]
Величина цикла исходного тиолактама оказывает влияние на характер протекания реакции. По-видимому, в случае пятичленного кольца положение таутомерного равновесия сильно сдвинуто в сторону меркаптидной формы. [34]
Такого рода сведения весьма ценны для химии гетероциклических соединений. Например, константы ионизации могут быть использованы при исследовании положения таутомерного равновесия ( см. раздел III, 4) и при установлении строения неизвестных веществ. [35]
Когда поверхность потенциальной энергии имеет два минимума, естественно возникает вопрос о высоте разделяющего их барьера и о скорости миграции протона между ними. Скорость перехода протона в принципе можно определить релаксационными методами, быстро смещая положение таутомерного равновесия путем изменения внешнего параметра и измеряя скорость релаксации системы. Однако в случае комплексов с водородной связью типа ОН - - N пока не известно ни одного примера успешного измерения такого рода. К такому же выводу приходят теоретикипри расчетах скоростипереходапротонаводно-мерных двойных потенциальных ямах с различными высотой барьера и расстоянием между ямами. Например, по данным работы [ 1271, при достаточно реальном расстоянии, которое необходимо пройти протону, возможно эффективное туннелирование е частотой порядка 1013 сек 1 даже через довольно высокий барьер - 5 ккал / моль над нулевым уровнем. [36]
Когда поверхность потенциальной энергии имеет два минимума, естественно возникает вопрос о высоте разделяющего их барьера и о скорости миграции протона между ними. Скорость перехода протона в принципе можно определить релаксационными методами, быстро смещая положение таутомерного равновесия путем изменения внешнего параметра и измеряя скорость релаксации системы. Однако в случае комплексов с водородной связью типа ОН - - N пока не известно ни одного примера успешного измерения такого рода. К такому же выводу приходят теоретики при расчетах скорости перехода протона в одномерных двойных потенциальных ямах с различными высотой барьера и расстоянием между ямами. Например, по данным работы [127], при достаточно реальном расстоянии, которое необходимо пройти протону, возможно эффективное туннелирование с частотой порядка 1013 сект1 даже через довольно высокий барьер - 5 ккал / молъ над нулевым ур овнем. [37]
Таутомерное равновесие обычно сдвигается в сторону форм с меньшей кислотностью. В ряду амидофосфатов XNHPO ( OR) 2 кислотность таутомерных форм и, следовательно, положение таутомерного равновесия должно зависеть, главным образом, от злектроотрицательности радикала X. Поэтому диэфиры арилсульфониламидофосфорных кислот должны быть описаны как особый тип фосфазосульфонилов. [38]
 |
Энергия резонанса о-хииоидиых гетероциклов, индола. [39] |
Таким образом, в чувствительной равновесной системе изоиндол - изоиндоленин близость энергий двух таутомерных форм отражает тот факт, что каждая из этих форм содержит лишь одно ароматическое кольцо, находящееся в сопряжении с полиеновой я-системой, дающем весьма незначительную дополнительную стабилизацию. Самые незначительные возмущения, которые могут повлиять на распределение электронной плотности, способны существенно изменить положение таутомерного равновесия. [40]
Ароматический характер гетероциклических соединений проявляется в ультрафиолетовых и инфракрасных спектрах. Спектральные исследования, особенно в УФ и видимой области, а также спектроскопия ядерного магнитного резонанса имеют чрезвычайно важное значение для оценки степени ароматичности соединений, определения положения таутомерного равновесия и изучения невыделяемых интермедиатов различных превращений. [41]
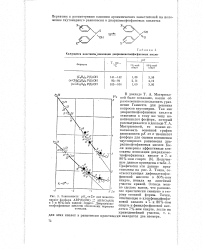
В докладе Т. А. Мастрюко-вой было показано, каким образом можно использовать уравнение Гамметта для решения вопросов таутомерии. Так как диарилтиофосфиновые кислоты относятся к тому же типу мо-нотиокислот фосфора, который рассматривается в докладе Т. А. Мастрюковой, то можно использовать основной график зависимости рК от а тиокислот фосфора для оценки положения таутомерного равновесия диарилтиофосфиновых кислот. Точка, соответствующая дифенилтиофос-финовой кислоте в 80 % - ном спирте, попала на линейный участок кривой. Отсюда можно сделать вывод, что равновесие практически смещено в сторону тионной формы. [43]
Проведено сравнение регионаправленности реакции ацилгидразинов с алканоилацетогетаренами и их трифторметильными аналогами, и изучена способность полученных продуктов конденсации к кольчато-цепным таутомерным превращениям. Для первой серии 1 3-дикетонов независимо от природы гетероароматического заместителя реакция протекает исключительно по алканоильной группе с образованием енгидразинов или 5-гидрокси - 2-пиразолинов, а для фторсодержащих дикетонов - по обеим карбонильным группам. Положение таутомерного равновесия сильно зависит от структуры дикетона. [44]
Положение таутоморного равновесия во всех случаях зависит от относительной основности ( или кислотности) форм в данной среде. При этом равгговесие, как ото следует ггл приведенных выше формул, всегда смещено в сторону менее основной ( или, соответственно, менее кислотной) формы. Так как соотношение констант ионизации зависит от природы растворителя, то и положение таутомерного равновесия зависит от природы растворителя. Эта зависимость выражается приведенными формулами. Если же одна из форм намного превышает другую по термодинамической константе ионизации, то равновесие во всех растворителях смещено в сторону этой: менее ионизируемой формы. [45]
Страницы: 1 2 3 4