Порат
Cтраница 1
Порат [20] проверил это выражение, используя приведенные в литературе значения Kd и молекулярного веса фракций декстрана. [1]
 |
Скорость адсорбции трипсина на частицах препарата соевый ингибитор трипсина-агароза в суспензиях, различной концентрации. [2] |
Порат и Кристиансен [32] рекомендуют специфические сорбенты в виде геля помещать в контейнеры с полупроницаемыми стенками, через которые могут свободно проходить растворенные вещества, но задерживаются крупные частицы. [3]
Порат и Флодин [18] в 1959 г. впервые показали возможность использования геля декстрана для обессоливания водного раствора белка. [4]
Порат) более прочны и надежны, чем стеклянные. В качестве электродов используют платановую проволоку номер 26, навитую вокруг толстых стеклянных палочек. [5]
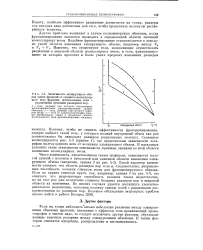 |
Зависимость элюирующего объема узких фракций от среднего молекулярного веса фракции. использованы гели с различными средними размерами пор. [6] |
Порату, наиболее эффективное разделение достигается на гелях, размеры пор которых едва достаточны для того, чтобы пропускать молекулы растворенного вещества. [7]
Порату [21 ] удалось достичь большего успеха в разделении белков, пептидов и аминокислот при использовании гелей декстранов, имеющих различное количество поперечных связей. [8]
Недавно Порат и Один описали синтез двух очень эффективных хелатных сорбентов. Первый из них - иминодпацетатсефароза ( IDA-Sepharose 6B) - способен фиксировать металл тремя координационными связями, а второй - трис ( карбоксиметил) этилендна-минсефароза ( TED-Sepharose 4B) - пятью. Элюцию белков с этих сорбентов можно осуществлять растворами аминокислот ( или их аналогов) - по-видимому, тех, которые взаимодействуют с металлом в составе белка. В работе приведены примеры очистки некоторых белков плазмы на колонках с хелированным никелел. Известно, что координационные связи белка с металлом усиливаются в присутствии высоких концентраций NaCl ( до 5 М), что облегчает борьбу с неспецифической адсорбцией белков. Такой же эффект дает присутствие в растворе этиленгликоля или диметилсульфоксида. [9]
Разработанная Поратом и Флодиным в 1959 г. [15] гель-фильтрация явилась большим достижением в развитии фракционирования белков по молекулярному весу. [10]
В 1959 г. Порат и Флодин [23] предложили новый тип хроматографии - гель-проникающую хроматографию: анализируемые растворы медленно фильтруются через колонки, заполненные частицами соответствующего геля. [11]
Допущения, сделанные Поратом и Сквайром относительно геометрической формы доступных областей геля, довольно произвольны; однако они вполне наглядно объясняют связь между параметрами элюиро-вания и молекулярным весом. Во всяком случае, тот факт, что выведенные уравнения подтверждаются экспериментом, говорит в пользу исходной концепции, согласно которой часть фазы геля недоступна Для молекул вещества. [12]
Допущения, предложенные Поратом относительно геометрической формы доступных областей геля, произвольны. Однако они удобны, так как достаточно наглядно объясняют связь между размерами частиц хроматографируемых веществ и параметрами их вымывания из колонки. Заметим, что выведенные уравнения, несмотря на сделанные допущения, достаточно удовлетворительно согласуются с экспериментом. [13]
В 1959 г. Флодин и Порат [30] получили продукт взаимодействия растворимого декстрана с эпихлор-гидрином; этот продукт оказался универсальным гелем, который вскоре начали вырабатывать в промышленных масштабах и выпускать в продажу под торпъ-вым названием сефадекс. [14]
Гель-хроматография предложена в 1959 г. Поратом и Фло-дином, аффинная хроматография - в 1967 г. Поратом, Аксеном и Эрнбеком. Различные варианты однофазной хроматографии были разработаны Гиддингсом. [15]
Страницы: 1 2 3 4