Нулевой порядок - реакция
Cтраница 1
Нулевой порядок реакции по молибдену ( У) означает, безусловно, то, что молибден не принимает участия в стадии, определяющей скорость реакции. [1]
Нулевой порядок реакции в отношении концентрации бромид-ионов свидетельствует о том, что они участвуют в стадии, скорость которой не является самой медленной. [2]
Нулевой порядок реакции можно объяснить, приняв, что в электрохимическом процессе участвует только активная часть поверхности, на которой скорость адсорбции Н2 достигает достаточной величины. На активной части поверхности имеет место адсорбционное равновесие с молекулярным водородом, соответствующее значительному заполнению, а скорость суммарного процесса определяется скоростью некоторой стадии, следующей за адсорбцией, например скоростью ионизации адсорбированного водорода или поверхностной диффузией атомов от центров, на которых происходит адсорбция, к центрам, на которых происходит ионизация. Таким образом, порядок реакции электрохимического окисления водорода зависит в основном от соотношения между скоростями различных стадий процесса. [3]
Здесь нулевой порядок реакции обусловлен почти полным покрытием поверхности, десорбция с которой идет с постоянной скоростью. [4]
Получаем нулевой порядок реакции и значение энергии активации 141 ккал / моль. [5]
Определен нулевой порядок реакции по Н2О2, энергия активации 12 ккал / моль. [6]
Мы объяснили нулевой порядок реакции сильной адсорбцией спиртов и считаем, что это же объяснение применимо и к настоящему случаю. [7]
Приведенное истолкование нулевого порядка реакции карбидирования по окиси углерода достаточно тривиально. Не вдаваясь в детали механизма, можно сделать довольно строгое заключение о том, что наличие нулевого порядка указывает на высокую концентрацию промежуточных комплексов с участием окиси углерода и на то, что лимитирующей стадией реакции являются дальнейшие превращения этих комплексов. [8]
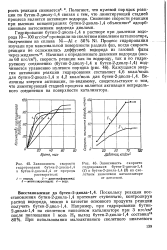 |
Зависимость скорости.| Зависимость скорости гидрирования бутен-2 - диола-1 4 ( 1 и бутин-2 - диола-1 4 ( 2 на скелетном никелевом катализаторе от давления. [9] |
Полагают, что нулевой порядок реакции по бутин-2 - диолу-1 4 связан с тем, что лимитирующей стадией процесса является активация водорода. [10]
Эти условия обеспечивают нулевой порядок реакции, при котором ее скорость лимитируется только концентрацией исследуемого фермента. [11]
Для расчета принимают нулевой порядок реакции самонагревания в материале и считают, что она подчиняется закону Аррениуса; кроме того, принимают, что материал изотропен и его физические и химические свойства не зависят от температуры. [12]
В работе [9 .35] предполагался нулевой порядок реакции и постоянная ее скорость. Удивительно, что с учетом этого существенного и мало реального упрощения были получены результаты, достаточно хорошо описывающие качественное поведение системы в процессе регенерации. [13]
В этом случае наблюдается нулевой порядок реакции по непредельному соединению и первый порядок по водороду. Энергии активации реакций практически одинаковы при гидрировании любых соединений и составляют 12 - 14 ккал / молъ, что характерно для процесса атомизации водорода. Скорость гидрирования таких соединений не зависит от рН раствора. [14]
Действительно, авторы принимают нулевой порядок реакции для всех случаев лишь на основе независимости изменений начальной скорости от давления в пределах 0 2 - 0 5 атм. [15]
Страницы: 1 2 3 4