Нулевой порядок - реакция
Cтраница 3
Преимущества этого метода перед другими состоят в следующем: при его применении сохраняется постоянное значение рН и, следовательно, нет опасности изменения активности фермента вследствие изменений его ионизации; метод сразу дает постоянную по большому числу точек кинетическую кривую, позволяющую рассчитывать необходимые кинетические константы ферментативной реакции; метод позволяет измерять кинетику процесса практически при любых условиях; расход времени на измерение скорости реакции весьма невелик; при условиях нулевого порядка реакции обычно бывает достаточно проводить титрование в течение 3 - 4 мин. [31]
Обычно считают, что при адсорбции ароматического соединения ненасыщенное кольцо его располагается плоско ( плашмя) на поверхности катализатора. Нулевой порядок реакции по отношению к концентрации гидрируемого исходного соединения обычно считают показателем сильной адсорбции. [32]
Для осуществления р О необходимо выполнение двух условий: во-первых, замедленность одной из стадий, следующих за адсорбцией, во-вторых, степень заполнения активной части поверхности должна быть близка к. Нулевой порядок реакции можно объяснить, приняв, что в электрохимическом процессе участвует только активная часть поверхности, на которой скорость адсорбции Н2 достигает достаточной величины. На активной части поверхности имеет место адсорбционное равновесие с молекулярным водородом, соответствующее значительному заполнению, а скорость суммарного процесса определяется скоростью некоторой стадии, следующей за адсорбцией, например скоростью ионизации адсорбированного водорода или поверхностной диффузией атомов от центров, на которых происходит адсорбция, к центрам, на которых происходит ионизация. Таким образом, порядок реакции электрохимического окисления водорода зависит в основном от соотношения между скоростями различных стадий процесса. [33]
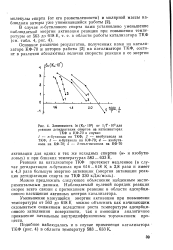 |
Зависимость 1п ( Ко - Ю4 от 1 / Г. 103для реакции дегидратации спиртов на катализаторах. [34] |
Наблюдаемый нулевой порядок реакции скорее всего связан с протеканием реакции в области адсорбционного насыщения активных центров катализатора. [35]
Отношение объемов возрастает с увеличением порядка реакции. Только для нулевого порядка реакции объемы одинаковы. [36]
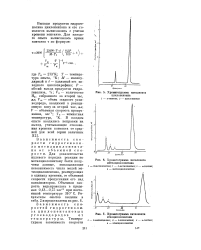 |
Хроматограмма катализата.| Хроматограмма катализата метилциклопентана.| Хроматограмма катализата. [37] |
Для доказательства нулевого порядка реакции по метилциклопентану были получены данные, показывающие независимость числа молей ме-тилциклопентана, реагирующих в единицу времени, от объемной скорости пропускания его над катализатором. [38]
В процессе реакции потенциал смещается в анодную-сторону на величину, при которой водород на поверхности практически отсутствует. При этом наблюдается нулевой порядок реакции по непредельному соединению и первый - по водороду. Энергия активации таких реакций характерна для процесса атомизации водорода, почти одинакова при гидрировании любых соединений и достигает 50 - 59 кДж / моль. Скорость их гидрирования не зависит от рН раствора. [39]
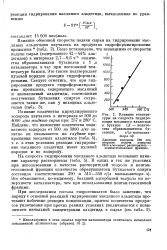 |
Влияние температуры на скорость гидрирования масляного альдегида в бутанол ( X - количество образовавшегося бу-танола, г / ( л катализа. [40] |
Было установлено, что независимо от скорости подачи сырья ( содержащего 42 - 44 % альдегидов) в интервале 2 7 - 8 6 ч 1 количества образовавшихся бутанолов с 1 л катализатора в час при постоянной температуре близки. Это также подтверждает нулевой порядок реакции гидроформилирования. [41]
В самом деле, в случае по крайней мере реакций с двуокисью углерода и с водяным паром при низких температурах и давлениях, не слишком отличающихся от атмосферного, найдено, что реакция подчиняется уравнению нулевого порядка. Как уже упоминалось, сущность нулевого порядка реакции состоит в том, что суммарная скорость газификации определяется скоростью удаления или перегруппировки комплекса поверхность - кислород в десорбирующийся продукт, но не скоростью его образования. Следовательно, энергия активации реакции - это энергия активации разрушения комплекса поверхность - кислород с выделением окислов углерода. [42]
 |
Принципиальная технологическая схеца противоточного процесса в трехступенчатом каскаде реакторов. [43] |
Существуют два предельных случая, когда противоточный процесс не имеет никаких преимуществ перед прямоточным. Если скорость выщелачивания не зависит от концентрации активного реагента ( нулевой порядок реакции), то интенсивность процесса в любой ступени совершенно не зависит от направления потоков. Точно так же обстоит дело, если скорость процесса не зависит от степени выщелачивания полезного компонента. Оба эти случая мало характерны для процессов растворения. [44]
На таком графике отчетливо выражена особенность кинетики ультразвукового разложения исследуемого вещества. Поскольку временная зависимость имеет линейный характер, то это означает нулевой порядок реакции. Сама реакция происходит только в водной среде, где постоянство концентрации растворенного исследуемого вещества обеспечивается достаточным его исходным количеством, превышающим растворимость в воде, поэтому порядок реакции и является нулевым, не зависящим от соотношения объемов органического вещества и воды. На рис. 2 и 3 показана зависимость кинетики разложения от мощности ультразвука и времени действия ультразвука. [45]
Страницы: 1 2 3 4