Нулевой порядок - реакция
Cтраница 2
Это характерно для соединений, имеющих нулевой порядок реакции по гидрируемому веществу. Следовательно, рост скорости гидрирования определяется активацией водорода. Значительное смещение потенциала при гидрировании, особенно на никеле, приводит к быстрой дезактивации катализатора, поэтому наиболее целесообразно работать при максимальной скорости в отсутствие избытка непредельного соединения в растворе. Рост смещения потенциала при накоплении продукта реакции позволяет рассчитать изотерму адсорбции р-фенилпропиолового спирта. Проведение реакции в таком же режиме при другой температуре позволяет рассчитать температурные коэффициенты оптимальной скорости и адсорбции продукта реакции. Так, например, при гидрировании диметилэтинилкарбинола на никеле при одинаковой заданной скорости, равной 4 8 мл Н2 в 1 мин. [16]
 |
Результаты расчетов по уравнениям ( V, ( VI и ( VII и опытные данные. [17] |
Выражение ( VII), дающее практически нулевой порядок реакции по концентрациям Н2 и 02, совершенно не согласуется с экспериментальными данными. [18]
Вначале кривая идет параллельно оси абсцисс ( нулевой порядок реакции), а затем начинает падать, подчиняясь уравнению реакции первого порядка. При увеличении в молекуле этилена числа заместителей горизонтальный участок кривой располагается все ниже, а падающая часть начинается все ближе к началу кривой, становясь более пологой. Так, например, у тетраметилэтилена кривая располагается очень низко и падение скорости практически происходит с самого начала реакции. При гидрогенизации смесей этиленов разной степени замещения получаются кинетические кривые ступенчатой формы. Вначале гидрогенизуется менее замещенный, а затем более замещенный компонент смеси. [19]
При концентрации ацетилхо-лина 5 05.1 СГ4 М нулевой порядок реакции сохраняется менее 1 мин. В связи с этим возникла идея создания метода, который позволял бы поддерживать в реакционной среде постоянство любой сколь угодно малой концентрации субстрата. [20]
Хотя формиат никеля при низких температурах достаточно стабилен, чтобы обеспечить нулевой порядок реакции, при более высоких температурах она становится реакцией первого порядка. [21]
В случае арилалкансульфонатов, в частности для 2-мезитилэтансульфоната натрия, был обнаружен нулевой порядок реакции нитрования и, соответственно, скорости образования NO2 в смесях, содержащих около 40 мол. Это является доказательством эффективности механизма, включающего нитроний-ион, даже в условиях, неблагоприятных для его проявления, которые, напротив, способствуют прямому взаимодействию других агентов ( например, H2NOsh) с ароматическим соединением. [22]
Для практических целей получения равномерных по толщине покрытий наибольший интерес представляет область нулевого порядка реакций. [23]
Что для нас особенно важно в табл. 29 - это то, что нулевой порядок реакции одновременно как по гидрируемому соединению, так и по водороду наблюдается очень часто, а это может быть объяснено только с точки зрения нашей теории, а именно с помощью уравнения (6.11), и никак не вытекает из прежних представлений, требующих квадрата в знаменателе кинетического уравнения. [24]
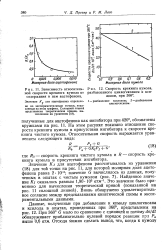 |
Скорость крекинга кумола, разбавленного циклогексаном и ксилолом, при 360.| Зависимость относитель. [25] |
При 360 G мало по сравнению с единицей и потому dn / dt обнаруживает приблизительно нулевой порядок реакции при Р выше 0 6 атм. [26]
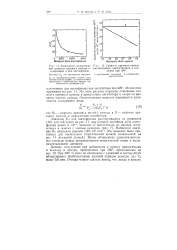 |
Скорость крекинга кумола, разбавленного циклогексаном и ксилолом, при 360.| Зависимость относитель. [27] |
При 360 G мало по сравнению с единицей и потому dn / dt обнаруживает приблизительно нулевой порядок реакции при Р8 выше 0 6 атм. [28]
При более высоких температурах скорость все еще первого порядка, но быстро уменьшается до температуры, где устанавливается нулевой порядок реакции; далее скорость снова возрастает, при этом энергия активации принимает более высокие значения. [29]
Скорость выцветания мономолекулярного слоя должна подчиняться тогда кинетическому закону первого порядка, в то время как для больших агрегатов следует ожидать нулевого порядка реакции. В случае систем, представляющих смеси дисперсного и агрегированного красителя, кинетические кривые должны отражать сначала быстрое падение скорости по экспоненциальному закону с последующим переходом в область более медленной реакции, протекающей с постоянной скоростью. Сравнение теоретических уравнений с экспериментальными данными привело этих авторов к выводу, что во всех изученных системах, за исключением водорастворимых красителей на такой гидрофобной подложке, как коллодий, красители были агрегированы. [30]
Страницы: 1 2 3 4