Общий порядок - реакция
Cтраница 1
Общий порядок реакции по исходным веществам - второй, а по веществам А или В - первый. [1]
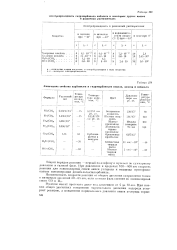 |
Физические свойства карбонилов и гидрокарбонилов никеля, железа и кобальта. [2] |
Общий порядок реакции - первый по олсфипу ц нуленом по суммарному давлению в газовой фазе. При давлениях в пределах 100 - 400 am спорость реакции для эквимолярпой смеси окиси углерода и водорода пропорциональна концентрации дикобальтоктакарбонила. [3]
Общий порядок реакции определяют экспериментально. Порядок может быть дробным, но для многих реакций он выражается целыми числами. [4]
Общий порядок реакции определяется порядком наиболее медленно идущей стадии. Таких стадий может быть несколько, и поэтому экспериментально определенный порядок реакции может быть дробной величиной. [5]
Общий порядок реакции равен сумме показателей степеней концентраций всех реагентов, которые входят в кинетическое уравнение для скорости реакции. [6]
Общий порядок реакции равен четырем, но ни один из частных порядков не превышает двух. [7]
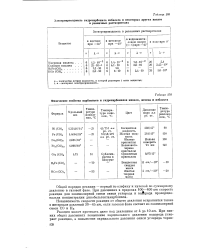 |
Физические свойства карбонилов и гидрокарбонилов никеля, железа и кобальта. [8] |
Общий порядок реакции - первый по олефину и нулевой по суммарному давлению в газовой фазе. При давлениях в пределах 100 - 400 am скорость реакции для эквимолярной смеси окиси углерода и водорода пропорциональна концентрации дикобальтоктакарбонила. [9]
Различают частный и общий порядок реакции. Частный порядок определяется по изменению концентрации одного из реагирующих веществ. Сумма частных порядков дает общий порядок реакции. Частный порядок находится несколькими методами. [10]
Как определяется общий порядок реакции. [11]
Следовательно, общий порядок реакции равен двум и согласуется с работами И, 2 ], в которых было показано, что щелочной гидролиз метил-и этилхлорацетата подчиняется уравнению второго порядка. Для расчета концентрации ионов ОН - в буферных растворах были приближенно определены коэффициенты активности f () H. При ионной силе / - 0 1 и 0 75 получены значения fOH 0 69 и 0 48, соответственно. [12]
Следовательно, кажущийся общий порядок реакции зависит от изменения величины ( 1 - 0р) со временем. Второй член правой части уравнения ( 8) первоначально близок к нулю, но затем становится все более отрицательным. Понижение скорости, обусловленное этим членом, суммируется с понижением первого порядка реакции, и это приводит к тому, что кажущийся общий порядок становится больше истинного. [13]
В этом случае общий порядок реакции не будет равен трем, а показатели степени в кинетическом уравнении не будут равны стехиометрическим коэффициентам в общем уравнении реакции. Показатели степени в кинетическом уравнении могут быть и дробными. [14]
Употребляется также выражение общий порядок реакции, что означает сумму частных порядков. [15]
Страницы: 1 2 3 4