Общий порядок - реакция
Cтраница 3
Тангенс угла наклона прямой дает значение общего порядка реакции п а отрезок отсекаемый прямой на оси ординат - значение константы скорости реакции. [31]
 |
Нахождение кинетических констант логарифмированием уравнений кинетики. [32] |
Тангенс угла наклона прямой дает значение общего порядка реакции п, а отрезок отсекаемый прямой на оси ординат - значение константы скорости реакции. [33]
Тангенс угла наклона прямой дает значение общего порядка реакции п, а отрезок, отсекаемый прямой на оси ординат, - значение константы скорости реакции. [34]
 |
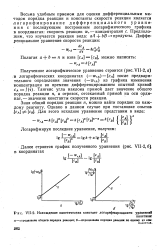
Нахождение кинетических констант логарифмированием уравнений кинетики. [35] |
Тангенс угла наклона прямой дает значение общего порядка реакции п, а отрезок отсекаемый прямой на оси ординат - значение константы скорости реакции. [36]
 |
Нахождение кинетических констант логарифмированием уравнений. [37] |
Тангенс угла наклона прямой дает значение общего порядка реакции п, а отрезок, отсекаемый прямой на оси ординат, - значение константы скорости реакции. [38]
Величина a - j - Р представляет собой общий порядок реакции, а и Р не обязательно целые числа. [39]
Полученный в результате графической обработки экспериментальных данных общий порядок реакции разложения NH4C1 гидроокисью кальция оказался близким к 3 0, а порядок реакции по гидроокиси кальция близок к единице. Таким образом, процесс соответствует уравнению ( 234) и определяющей скорость процесса разложения NH4C1 стадией является химическая реакция. [40]
Для того чтобы при первом порядке реакции инициирования общий порядок реакции был полуторным, нужно, чтобы обрыв цепей осуществлялся при взаимодействии двух радикалов, участвующих в реакции продолжения цепи, имеющей второй порядок. [41]
Сумма показателей степеней р q, определенных экспериментально, дает общий порядок реакции. [42]
Опытные точки действительно ложатся на прямую, что подтверждает второй общий порядок реакции. [43]
Сумма показателей степеней при концентрациях реагирующих веществ в кинетическом уравнении определяет общий порядок реакции. [44]
 |
Зависимость начальной скорости разложения кумилгидроперекиси в присутствии бромистого N-цетил - З - карбамидопиридиния ( рН 9. 90 С от концентрации гидроперекиси. [45] |
Страницы: 1 2 3 4