Общий порядок - реакция
Cтраница 2
Показать, что общий порядок реакции равен двум, и вычислить константу скорости. [16]
Для того чтобы найти общий порядок реакции П П целесообразно взять реагенты в стехиометрическом соотношении. [18]
При температуре 225 С общий порядок реакции остается первым, но начальная скорость ниже, чем при температуре 210 С. При 250 и 300 С порядок реакции приближается к нулевому, что может быть объяснено активацией катализатора водородом. Выше 300 С восстановление катализатора выражено настолько резко, что не позволяет провести интерпретацию кинетических результатов. [19]
Сумма частных порядков представляет собой общий порядок реакции. [20]
Размерность констант скорости зависит от общего порядка реакции р и единиц выражения концентрации С. [21]
 |
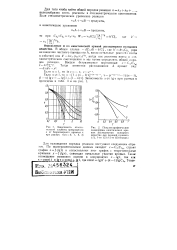
Кривые Аррениуса для низкотемпературных образцов чистой и промотированной окиси цинка при постоянной начальной скорости. [22] |
В интервале 80 - 125 С общий порядок реакции, измеренный на ZnO ( Li), изменяется с температурой от 0 7 до 1 0, в то время как порядок реакции на ZnO ( Ga) остается равным единице. [23]
KC ciroii кислоте, определен второй общий порядок реакции, маетные порядки по амину и азотистой кислого и энергия активации. [24]
 |
Кривые Аррениуса для низкотемпературных образцов чистой и промотированной окиси цинка при постоянной начальной скорости. [25] |
В интервале 80 - 125 С общий порядок реакции, измеренный на ZnO ( Li), изменяется с температурой от 0 7 до 1 0, в то время как порядок реакции на ZnO ( Ga) остается равным единице. [26]
Величина а 4 - р представляет собой общий порядок реакции, а и Р не обязательно целые числа. [27]
 |
Нахождение кинетических констант логарифмированием уравнений кинетики. [28] |
Тангенс угла наклона прямой дает значение общего порядка реакции п, а отрезок отсекаемый прямой на оси ординат - значение константы скорости реакции. [29]
 |
Нахождение кинетических констант логарифмированием уравнений кинетики. [30] |
Страницы: 1 2 3 4