Концевая последовательность
Cтраница 3
Поскольку в большинстве гликопротеинов углеводная часть является определяющей для проявления специфической биологической активности, очень важное место в установлении концевой последовательности олиго-сахаридных цепей играют иммунохимические методы, которые одновременно позволяют непосредственно определить и структуру антигенных детерминантов. Этот путь играет особенно большую роль в исследовании гликопротеинов и оказался весьма плодотворным при изучении групповых веществ крози. [31]
Формула ао является предикатной тавтологией в том и только в том случае, когда диаграмма для о конечна и все концевые последовательности фундаментальны. [32]
Формула о является предикатной тавтологией в том и только в том случае, когда диаграмма для аи конечна и все концевые последовательности фундаментальны. [33]
Из всех этих соображений следует, что если диаграмма для о конечна, то формула а0 является предикатной тавтологией в том и только в том случае, когда все концевые последовательности в ее диаграмме являются фундаментальными. [34]
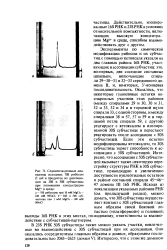 |
Седиментационные диаграммы исходных 70S рибосом Е. coli и продуктов их диссоциации на 30S и 50S субчастицы при понижении концентрации Mg2 в среде. [35] |
Эксперименты по химической модификации рибосом и их субчастиц с помощью кетоксаля указали на два главных района 16S РНК, участвующих в ассоциации субчастиц: это, во-первых, две соседние составные шпильки, включающие спирали 29 - 30 - 31 и 32 - 33 серединного домена II, и, во-вторых, З - концевая последовательность. Оказалось, что некоторые гуаниловые остатки неспаренных участков этих районов ( между спиралями 29 и 30, 30 и 31, 32 и 33, 32 и 34 и в торцевой педле спирали 33, с одной стороны, и между спиралями 38 и 57, 57 и 59 и в торцевой петле спирали 59, с другой) реагируют с кетоксалем в изолированной 30S субчастице и перестают реагировать после ассоциации с 50S субчастицей. Если эти остатки модифицированы кетоксалем, то 30S субчастица теряет способность к ассоциации с 50S субчастицей. Интересно, что ассоциация с 50S субчастицей вызывает также некоторую перестройку структуры РНК в 30S субчастице, приводящую к увеличению доступности нуклеотидных остатков в районе составной спирали 45 46 - 47 домена III 16S РНК. [36]
Как и в случае 16S ( 18S) РНК, довольно протяженная З - концевая последовательность 23S ( 28S) РНК не входит в состав главных доменов, а лишь образует несколько спиральных шпилек. В рибосомах хлоро-пластов высших растений 100-нуклеотидная З - концевая последовательность в цепи 23 S РНК отсутствует и представлена в виде отдельной цепочки 4 5S РНК. РНК складывается в две шпильки ( одна простая и одна составная из двух спиралей), гомологичные ( даже почти идентичные) 3 -концевым шпилькам 23S РНК бактерий. [37]
Путь а ( как при использовании чисто химических средств, так и при комбинированном использовании химических реакций и ферментов) предъявляет очень жесткие, практически в настоящее время еще недостижимые требования к специфичности и количествен-ности протекающих химических и ферментативных реакций. Поэтому данный путь используется пока лишь для определения сравнительно коротких концевых последовательностей или для установления строения олигонуклеотидов, содержащих до десяти нук-леотидных остатков. [38]
 |
Схема поздней ( рекомбинацнонкой инициации цепей ДНК фага Т 4. [39] |
В результате первого раунда репликации возникают два дочерних дуплекса с одноцепочечными З - концэ. Поэтому если клетка заражена несколькими фаговыми частицами, то концевая последовательность одной молекулы фаговой ДНК будет соответствовать внутреннему участку другой молекулы. При помощи специальных фагоспецифических белков одноцепочечный 3 -конец первой молекулы может внедриться во внутренний район другой молекулы; в результате появляется затравка, способная обеспечить дальнейшее удлинение цепи. В конечном счете возникает молекула, которую можно рассматривать как разветвленный конкатемер. Отметим, что рекомби-национная инициация имеет место и тогда, когда клетка заражается единственной фаговой частицей ( рекомбинация в этом случае происходит между одинаковыми дочерними молекулами. [40]
В этих уравнениях в целях упрощения не учтены реакции атаки на концевые последовательности. Это упрощение не может внести существенной ошибки, если длина цепи сополимера значительно больше длины последовательности звеньев. [41]
Другой ключевой фермент, широко применяемый для соединения фрагментов ДНК-это терминальная трансфе-раза, которая способна присоединять к 3 -концу цепей ДНК большое число следующих друг за другом дезоксирибону-клеотидных остатков. Поскольку для действия терминальной трансферазы не нужна матрица, она способна построить З - концевые последовательности, состоящие из нуклеотидов одного типа. Следовательно, к З - концам одной из двухцепо-чечной ДНК можно добавить poly ( G хвосты, а к З - концам другой - poly ( С хвосты. [43]
Можно отметить, что олигонуклеотид 11, как и укороченные последовательности, заканчивается пиримидином. Принимая, что / 3-гемоглобиновая мРНК оканчивается кодоном, соответствующим последней аминокислоте, можно ожидать, что эта концевая последовательность будет обнаружена во фракциях по длине цепи, содержащих 6, 12 или 14-меры, при условии если концевой Y фосфорилирован. Если же этот Y нефосфорилирован ( или если фосфат удален перед действием Т1 - РНК-азы), то концевую последовательность можно обнаружить во фракциях, содержащих 5, 11 или 13 отрицательных зарядов. [44]
Очень интересные возможности установления первичной структуры углеводсодержащих биополимеров открывает принцип индуцирования экзоферментов, который был предложен в работах Стейси и Баркера. Если этот принцип окажется достаточно универсальным, а его аналитическое оформление будет хорошо разработано, он может оказаться очень полезным для анализа концевых последовательностей в полисахаридных цепях. [45]
Страницы: 1 2 3 4
