Потенциал - коррозия
Cтраница 2
Понижение потенциала коррозии олова, когда концентрация олова в растворе понижается из-за образования комплексных ионов, было рассмотрено в разделе 2.6. Железо также может образовывать комплекс и на потенциал железа может действовать присутствие ионов олова в растворе. Область смещения потенциалов [4] зависит от процесса ком-плексообразования присутствующих агентов, концентрации и рН раствора. Взаимоотношения электрохимических характеристик олова и железа являются сложными, однако для практических целей олово может быть рассмотрено как анод по отношению к железу в контакте с такими продуктами, как фруктовые соки, мясо, мясные продукты и молоко, в растворах кислот лимонной, яблочной, винной, щавелевой и их солей, а также в щелочных растворах. В растворах неорганических солей, природной воде или в атмосферных осадках олово является катодом по отношению к железу. [16]
 |
Установка для проведения поляризационных измерений. [17] |
При потенциале коррозии протекает равновесное растворение поверхности металла. [18]
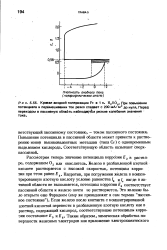
Это смещает потенциал коррозии до фа - D. Кривая ABC - парциальняя анодная кривая корродирующего металла, кривая DEGH - кривая катодного процесса. [19]
Первоначально измеряют потенциал коррозии в отсутствие тока Екор. Потом электрод катодно поляризуют в течение 30 секунд при потенциале на 200 мВ отрицательнее Екор. После этого снимают анодную поляризационную кривую при скорости развертки потенциала 10 мВ / с. Фиксируют величины токов с помощью миллиамперметра или высокоомного вольтметра. [20]
При 100 потенциал коррозии стали Х18Н10Т равен - 0 15 в, скорость коррозии без защиты около 22 г / м2 - ч; пассивация стали происходит при потенциале - 0 08 в. [21]
Несмотря на активный потенциал коррозии, сплав, например, содержащий 15 % Мо, корродирует в 12 раз медленнее никеля в деаэрированной 10 % - ной НС1 при 70 С. [22]
Еральв - потенциал коррозии гальванической пары ( измеренный на расстоянии, значительно превышающем размеры пары); ( 3 и / 0 - константа Тафеля и плотность тока обмена для разряда иона водорода на благородном металле. [23]
Метод определения потенциала коррозии может быть использован для испытаний готовых изделий и конструкций в производственных условиях. [24]
 |
Универсальный зонд для проведения 5 электрохимических исследований в грунтах. [25] |
Для определения потенциала коррозии используются рабочий электрод и электрод сравнения. [26]
 |
Нулевые точки некоторых металлов в воде и работа выхода электрона в вакуум. [27] |
Иными словами, потенциалы коррозии цинка и железа в приведенной шкале оказываются одинаковыми. Условия адсорбции ингибиторов на этих металлах должны быть примерно одинаковыми, так как близки их заряды. В то же время на железе следует ожидать несколько меньшего ингибирующего эффекта, чем на цинке, вследствие конкуренции ингибитора с уже адсорбированным атомарным водородом, которого почти нет на поверхности цинка. [28]
В большинстве случаев потенциал коррозии цинка отрицательный по сравнению со сталью, в частности в морской - и пресной природной воде при комнатной температуре. Однако в пресной воде ( хотя цинк и является анодом по отношению к стали) при температуре выше 60 С происходит перемена полярности: цинк становится катодом, что предопределяет коррозию в местах нарушения сплошности покрытия. [29]
Страницы: 1 2 3 4 5