Потенциал - коррозия
Cтраница 4
На рис. 3 показана зависимость потенциала коррозии от времени и анодные поляризационные кривые экономнолегироваяннх сталей в щелочном хлоридно-сульфатном растворе при концентрации щелочи 6 г / л, что соответствует содержанию щелочи при нормальном режиме процесса кристаллизации сульфата натрия. Из рис. 3 следует, что разница между стационарным потенциалом и потенциалом активации достаточно велика ( 0 5 0 25 В), то есть все стали в таком растворе должны обладать устойчивостью к локальной коррозии. Сталь 08Х18Г8Н2Т менее устойчива к локальной коррозии ( потенциал ее активации ионами хлора более отрицателен), возможно, в связи с более низким содержанием никеля. [46]
При большом смещении потенциалов относительно потенциала коррозии фс общая поляризационная диаграмма совпадает с частными. [47]
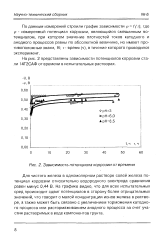 |
Зависимость потенциала коррозии от времени. [48] |
На рис. 2 представлены зависимости потенциалов коррозии стали 14Г2САФ от времени в испытательных растворах. [49]
Этот потенциал называется стационарным или потенциалом коррозии. [50]
В активной области и при потенциале коррозии сразу после погружения образуется смешанный оксид, но он не является защитным. [51]
Когда коррозионное растрескивание происходит при потенциале коррозии, добавки к коррозионной среде могут сдвинуть потенциал за пределы области коррозионного растрескивания и, таким образом, предотвратить растрескивание. И наоборот, когда потенциал коррозии находится вне области потенциалов, соответствующих коррозионному растрескиванию, тогда определенные добавки к коррозионной среде могут способствовать растрескиванию вследствие сдвига потенциала коррозии в область критических потенциалов. Такой подход позволяет разрешить многие противоречивые данные опубликованных работ. Эти наблюдения подтверждают действие добавок еще и тем, что при добавке к раствору NaOH таких веществ, как KMnO4, NaNO3 и Na2Cr04 наблюдается коррозионное растрескивание при температуре кипения, а при 250 С коррозионное растрескивание отсутствует, так как добавки уже действуют как ингибиторы. [52]
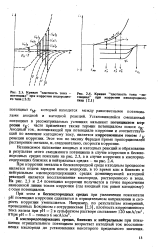 |
Кривая плотность тока - Ряс. 2А. Кривая плотность тока - по-потенциал при коррозии водородно - тенциал при коррозии кислородного го типа типа. [53] |
Анодный ток, возникающий при потенциале коррозии и соответствующий по величине катодному току, является коррозионным током z тг-реакции коррозии. Этот ток по закону Фарадея прямо пропорционален растворению металла, и, следовательно, скорости коррозии. [54]
На рис. 4.7 а показано изменение потенциала коррозии от фазового состава сплавов. Однако зависимость потенциала пассивации при возникновении новой фазы резко изменяет свой ход. [55]
Сравнение значений стационарных потенциалов железа ( потенциалов коррозии) в нейтральных электролитах ( - 0 3 - - 0 4 В) со значениями потенциалов образования окислов железа приводит к выводу, что уже при незначительном смещении потенциала железа или стали в положительную сторону от стационарного параллельно процессу ионизации металла на электроде должна протекать реакция окисления, приводящая к возникновению на поверхности окисных слоев. [56]
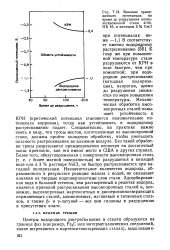 |
Влияние приложенного потенциала на время до разрушения низколегированной. стали 4140, HR 46, в кипящем 3 % NaCl. [57] |
КРН ( критический потенциал становится положительнее потенциала коррозии), тогда как устойчивость к водородному растрескиванию падает. Следовательно, на практике важно иметь в виду, что тросы мостов, изготовленные из высокопрочной стали, должны пройти холодную обработку, чтобы уменьшить опасность растрескивания во влажном воздухе. Без такой обработки тросы разрушаются преждевременно несмотря на достаточный запас прочности, как это имело место в США и других странах. NaCl, но быстро растрескивается при катодной поляризации. Назначительное количество водорода, образованного в результате реакции железа с водой, не оказывает влияния на твердые подповерхностные слои стали. Адсорбированная вода в большей степени, чем растворенный в решетке водород, является причиной растрескивания высокопрочных сталей и, возможно, высокопрочных мартенситных и дисперсионнотвердеющих нержавеющих сталей, алюминиевых, магниевых и титановых сплавов, а также J - и у-латуней - все они склонны к разрушению в присутствии влаги. [58]
Другой метод основан на определении изменения потенциала коррозии стали при. [60]
Страницы: 1 2 3 4 5
