Потенциал - коррозия
Cтраница 3
Рассмотрим теперь значение потенциала коррозии Е2 в растворе, содержащем 02 или окислитель. [31]
Екор, называемом потенциалом коррозии, наступает состояние равновесия. [32]
Этот потенциал определяется как потенциал коррозии. [33]
В случае имплантации Pd потенциал коррозии титана от значений - 0 44 В сильно смещается в положительную сторону. При условной толщине слоя Pd в 2 - 18 нм отмечены устойчивая пассивность и коррозионная стойкость титана в 20 % - ном растворе H2SO4 при 100 С. [34]
Поляризационные кривые получают регистрацией потенциала коррозии и коррозионного тока с помощью двухкоординатно-го самопишущего прибора с логарифмическим преобразователем. Определяют плотность коррозионного тока, пропорциональную скорости коррозии исследуемого металла, экстраполяцией участка Тафеля до значения потенциала коррозии на поляризационной кривой. [35]
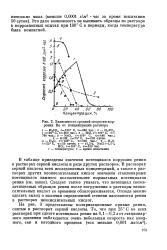 |
Зависимость средней скорости коррозии Re от концентрации раствора. [36] |
В таблице приведены значения потенциалов коррозии рения в растворах серной кислоты и ряде других растворов. Следует также указать, что потенциал свежезачищенных образцов рения после погружения в растворы неокислительных кислот со временем облагораживается. [37]
Какое значение потенциала называют потенциалом коррозии и как его устанавливают. [38]
Устанавливающиеся значения потенциала называют потенциалом коррозии Екор. [39]
 |
Пояснение методов защиты. [40] |
В большинстве случаев при этом потенциал коррозии находится в активной области [ фкорр ( 1) 1 или в области нарушения пассивности [ фкорр ( 2 ] ( рис. V. Добиться требуемого смещения потенциала без изменения кривой iCT / ( ф) можно при помощи элек - р трохимической защиты - i поляризации металла от 1 внешнего источника тока или за счет соединения с электродом ( протектором), который имеет в данной среде потенциал, заметно отличающийся от фкорр, и сравнительно низкую поляризуемость. [41]
Ряд экспериментальных данных ( установление потенциала коррозии, изменение перенапряжения выделения водорода в гальвяно-статических условиях) подтверждает вывод о селективном растворении титана и о накоплении катодного компонента на поверхности сплава. Для некоторых композиций сплавов на основе исследования кинетики накопления на поверхности более электроположительного элемента, рассчитана площадь поверхности сплава, занятая этим легирующим компонентом. [42]
Лф - IiRnifSt - изменение потенциала коррозии под действием поляризующего тока; Rnt - удельная поляризуемость металла, зависящая от плотности поляризующего тока /; Rpi - сопротивление растеканию тока; r ki и ты - - функции влияния, численно равные потенциалу, который возникает на отрезке с номером под действием единичного тока, соответственно стекающего с отрезка с номером k и его зеркального отражения относительно поверхности земли. [43]
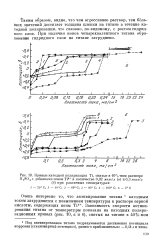 |
Кривые катодной поляризации Ti, снятые в 40 % - ном растворе. [44] |
Под активированием титана подразумевается достижение потенциала коррозии ( стационарный потенциал), равного приблизительпо - 0 41 в и ниже. [45]
Страницы: 1 2 3 4 5