Потенциал - металл
Cтраница 2
Потенциал металла остается более положительным, чем потенциал выделения водорода при сравнительно малых значениях плотностей тока, но, начиная с некоторого значения плотности тока, катодный потенциал становился отрицательнее потен -, циала выделения водорода. В этом случае при тех плотностях тока, при которых катодный потенциал не достигает потенциала выделения водорода, выделяется только металл. [17]
Потенциал металла, возникший при погружении металла в одно-нормальный ( 1 и. [18]
Потенциал металла зависит от природы металла, концентрации раетвора соли этого металла и температуры раствора. Потенциалы металлов, погружен ных в растворы их солей с концентрацией 1 моль / л, называют стйндартными электродными потенциалами. Значения стандартных электродных потенциалов различных металлов определяют по отношению к водородному электроду, потенциал которого условно принят равным нулю. [19]
Потенциал металла, погруженного в неизвестный раствор, прямо пропорционален величине рн. [20]
Потенциал металла или сплава, покрытого окисной пленкой, можно рассматривать также аналогично потенциалу многоэлектродного элемента. [21]
Потенциалы металлов в воде, конечно, отличны от их потенциалов в стандартных условиях; в большинстве случаев они имеют более отрицательное значение. Но, как правило, это не сказывается на правильности выводов о способности металлов вытеснять водород из воды. [22]
 |
Схема двойного электрического слоя ( плоская модель. а - 11Сц2, раств. 1Си2. мет. б-ц Сц2, раств. ИСи2. мет. [23] |
Потенциал металла в нулевом растворе Нернст определяет как абсолютный нуль потенциалов. [24]
Потенциалы металлов, находящихся в электрохимическом равновесии с нормальным раствором их ионов, называются нормальными или равновесными. [25]
Потенциал металла сложным образом зависит от концентрации иона в растворе. [26]
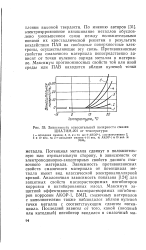 |
Зависимость относительной полярности смазки ЦИАТИМ-201 от температуры. [27] |
Потенциал металла сдвинут в положительную или отрицательную сторону, в зависимости от электронодонорно-акцепторных свойств данного смазочного материала. Зависимость противоизносных свойств смазочного материала от потенциала металла имеет вид классической электрокапиллярной кривой. Аналогичная зависимость показана [124] для защитных свойств маслорастворимых ингибиторов коррозии и ингибированных масел. [28]
Потенциал металла, помещенного в раствор своих собственных ионов, концентрация которых составляет 1 Г - моль / л, называется нормальным потенциалом данного металла. Нормальный потенциал металла по сравнению с потенциалом нормального водородного электрода, принятого за нуль, может быть положительным или отрицательным. [29]
Потенциалы металлов в нулевых растворах по отношению к стандартному электроду, так называемые потенциалы нулевого заряда, или нулевые точки металлов, по Фрумкину, могут быть измерены разными методами, которые основаны на наблюдении за зависимостью адсорбционных явлений от заряда поверхности. [30]
Страницы: 1 2 3 4