Потенциал - питтингообразование
Cтраница 4
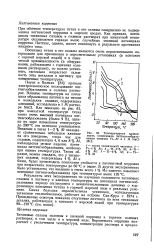 |
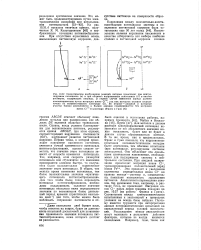
Температурная зэвиси-мость потенциала питтингообразования сплавов Ti-AI в 1 М NaCl. [46] |
Результаты этих экспериментов по изучению склонности титановых сплавов к питтингу и влияния температуры на потенциал питтингообразования хорошо согласуются с немногочисленными данными о коррозионном поведении титана в горячей морской воде в реальных условиях. [47]
Структурный фактор, однако, не сказывается на отчетливо выраженном отрицательном влиянии марганца на потенциал питтингообразования и скорость ПК в хлорном железе. [48]
Кривая Ti в условиях щели показывает, что потенциал начала развития щелевой коррозии отрицательнее потенциала питтингообразования на 1 2 В. Таким образом, можно сказать, что результаты исследо-тания электрохимического поведения Ti при температуре 160 С указывают на вероятность коррозии и в щели, и в объеме раствора, однако инкубационный период начала коррозионного процесса в щели значительно меньше, чем в объеме. [49]
Молибден, который является стабилизатором ферритной фазы, способствует пассивации стали ( повышает нижнюю границу потенциала питтингообразования) и тем самым повышает коррозионную стойкость. Добавка Мо способствует также повышению анодной поляризуемости, возможно, вследствие адсорбции на поверхности стали образующихся продуктов коррозии, но механизм действия Мо, очевидно, иной, чем у Ni, так как молибден не только уменьшает питтингообразование, но и снижает вероятность подповерхностной коррозии. [50]
В других экспериментах было установлено, что введение в титан всего 1 % Мо заметно повышает потенциал питтингообразования при температурах выше 125 С. [51]
Метод дает возможность определять минимальное положительное значение потенциала, при котором начинается активирование поверхности стали ( потенциал питтингообразования), а также получать другие количественные данные, позволяющие, с одной стороны, охарактеризовать способность стали сопротивляться активирующему влиянию галоидных ионов, а с другой - пассивирующие свойства различных анионов. По этому методу образец нержавеющей стали заряжается анодно при постоянном значении тока ( 2 - 5 мка / см2) и на автоматическом потенциометре записывается потенциал электрода. Если сталь подвергается питтинговой коррозии, на кривой заряжения появляются характерные колебания потенциала. [53]
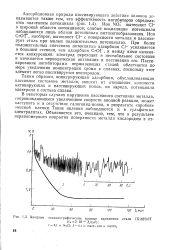 |
Анодные осциллографические кривые заряжения стали IX18H10T. [54] |
Ион NCb вытесняет С1 - в широкой области потенциалов; слабые осцилляции потенциала наблюдаются лишь вблизи потенциала питтингообразования. Ион CrOl, наоборот, вытесняет С1 - с поверхности металла и пассивирует сталь при малых положительных потенциалах. Пассивирование ингибиторами нержавеющих сталей облегчается по мере увеличения концентрации хрома в сплавах, поскольку этот элемент легко пассивируется кислородом. [55]
 |
Зависимость скорости коррозии СтЮ ( / и СтЮ с термодиффузионным покрытием цинка ( 2 от температуры. [56] |
Для коррозионного поведения нержавеющих сталей в морской воде характерна склонность к питтинговой коррозии, начало которой определяет значение потенциала питтингообразования. [57]
Даже нескольких дней бывает мало, чтобы ответить на вопрос, будет ли длительность испытаний достаточной для установления правильного значения потенциала питтингообразования, ниже которого питтинг не развивается. [59]
Узкая область потенциалов, при которой наблюдается резкое увеличение силы тока ( рис. 4, кривая Б), соответствует потенциалу питтингообразования. Явление питтингообразования характерно и для металлов, не подвергающихся окислению с образованием ионов более высокой степени окисления. [60]
Страницы: 1 2 3 4