Потенциал - полуволна - восстановление
Cтраница 1
Потенциалы полуволны восстановления всех карбонильных соединений становятся менее отрицательными при введении электроотрицательных заместителей. Эти эффекты могут быть количественно описаны с помощью уравнений Гаммета, Тафта и Юкава - Цуно с учетом стерических факторов. [1]
Потенциал полуволны восстановления всех углеводородов не зависит от рН раствора; поэтому при полярографировании углеводородов можно не пользоваться буферными растворами. [2]
Потенциал полуволны восстановления практически не зависит от рН раствора и природы г г фона. [3]
Потенциал полуволны восстановления комплекса должен быть отрицательнее, чем потенциал полуволны свободного иона, так как при восстановлении катион должен освободиться от лигандов, что связано с затратой энергии. [4]
Потенциал полуволны восстановления кислорода до Н2О2 незначительно зависит от среды и составляет примерно - 0 2 В. Вторая волна растянута и. [5]
Потенциал полуволны восстановления комплекса должен быть отрицательнее, чем потенциал полуволны свободного иона, так как при восстановлении катион должен освободиться от лигандов, что связано с затратой энергии. [6]
Потенциалы полуволн восстановления ионов соответственно равны - 0 3, - 0 8 и-1 35 е ( отн. [7]
Потенциал полуволны восстановления Pu ( IV) в Pu ( III), соответствующий максимуму на дифференциальных квадратно-волновых полярограммах, найден равным 0 71 в относительно пас. [8]
Потенциал первой двухэлектронной полуволны восстановления Е / 2 - 0 2 - гО 5 В в зависимости от рН среды. [9]
Потенциалы полуволн восстановления насыщенных альдегидов близки к 1 8 в и их раздельное определение в смесях невозможно; альдегиды, имею-шие двойную связь в а, р-положении к карбонильной группе, и ароматические восстанавливаются при менее отрицательных потенциалах, однако раздельное определение насыщенных и ненасыщенных соединений на фоне хлоридов и гидроокисей затруднено. [10]
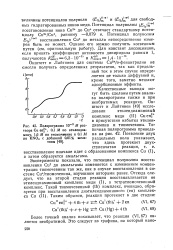
По потенциалам полуволны восстановления Си ( I) - Си ( о) при различных концентрациях углеводорода ( С /) была построена зависимость Ei / 2 - Ifi Ci. [11]
Эксперименты показали, что потенциал полуволны восстановления Си1 до амальгамы изменяется с изменением концентрации тиомочевины так же, как в случае восстановления в системе Си / тиомочевина, изученном авторами ранее. Отсюда следует, что на второй стадии реакции восстанавливается не этилендиаминовый комплекс меди ( I), а тетратиомочевинный комплекс. [13]
Особенно большое влияние па потенциал полуволны восстановления бромата оказывает рН, так как ионы Н участвуют в электродной реакции. [14]
В табл. 4 приведены значения потенциала полуволн восстановления различных бромсодержащих органических веществ. Из данных таблицы видно, какое большое влияние на потенциал полуволны оказывает положение брома в молекуле. [15]
Страницы: 1 2 3 4