Потенциал - полуволна - восстановление
Cтраница 3
 |
Кривая анодного растворения металла из амальгамы и способ ее намерения. [31] |
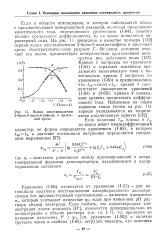
Для определения одного или нескольких элементов на электроды накладывают напряжение, превышающее потенциал полуволны восстановления наиболее электроотрицательного элемента на 0 2 - 0 3 В. При этом напряжении в течение заданного времени проводят электролиз исследуемого раствора при его перемешивании. Затем после успокоения раствора снимают подпрограмму анодного растворения металлов из амальгам при непрерывно уменьшающемся потенциале. [32]
 |
Волна восстановления. [33] |
Уравнение ( 1 - 66) отличается от уравнения ( 1 - 51) - для потенциала полуволн восстановления адсорбированного деполяризатора без предшествующей протонизации - наличием множителя as, который учитывает изменение ф1 / 2 волн при изменении рН раствора вблизи электрода. Если считать, что приэлектродная концентрация ионов водорода [ H ] s изменяется пропорционально их концентрации в объеме раствора ( см. гл. [34]
В основе метода лежит реакция образования мышьяком ( Ш) полярографически активного комплекса с винной кислотой, потенциал полуволны восстановления которого составляет - 1 16 в. Титрование проводят на фоне 0 1 М H2S04 в присутствии 20 % этанола и 0 005 % желатина. [35]
 |
Потенциалы расщепления связи углерод - галоген ( Е п, в. [36] |
Проведенные расчеты качественно согласуются с экспериментальными данными, как это можно видеть из табл. 38, где представлены потенциалы полуволн восстановления некоторых простейших галогенсодержащих соединений. [37]
Количественное полярографическое измерение таких кетонов, связанное с рядом помех, не имеет большого значения; в данном случае важнее измерение потенциалов полуволны восстановления, позволяющее установить особенности строения изучаемого кетона. [38]
Однако анионная полимеризация стирола [112] в гексаметилтриамидо-фосфате, содержащем MeJSlBPli не допускает различных толковании, так как в этих условиях разряд катиона происходит при потенциале на 40 мВ более отрицательном, чем потенциал полуволны восстановления стирола. [39]
При изучении вольтамперометрического поведения 1-пирроли-динкарбодитионатных комплексов марганца ( III), железа ( III) и меди ( II) в неводных растворителях выявлено закономерное изменение величин разности потенциала полуволны окисления и потенциала полуволны восстановления в зависимости от сольватирующих параметров растворителей. [40]
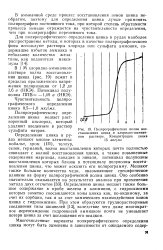 |
Полярографическая волна восстановления цинка в хлоридно-аммиачном растворе. Концентрация цинка 15 мкг / мл. [41] |
Определению цинка в ру-цах мешают многие элементы: кобальт, хром ( III), теллур, селен, германий, волна восстановления которых почти полностью совпадает с волной восстановления цинка, а также повышенные содержания марганца, ванадия и никеля, потенциал полуволны восстановления которых близок к потенциалу полуволны восстановления цинка, что может исказить его подпрограмму. Мешают также большие количества меди, оказывающие специфическое влияние на форму полярографической волны цинка. Определению цинка мешает также большое содержание в пробе железа и алюминия, с гидроокисями которых заметно соосаждаются ионы цинка как, по-видимому, за счет их сорбции, так и за счет химического взаимодействия ионов цинка с гидроокисями. При этом образуются труднорастворимые соединения типа шпинелей [13], вследствие чего даже многократное переосаждение гидроокисей аммиаком почти не уменьшает потери цинка за счет поглощения его осадком. [42]
Определению цинка в ру-цах мешают многие элементы: кобальт, хром ( III), теллур, селен, германий, волна восстановления которых почти полностью совпадает с волной восстановления цинка, а также повышенные содержания марганца, ванадия и никеля, потенциал полуволны восстановления которых близок к потенциалу полуволны восстановления цинка, что может исказить его подпрограмму. Мешают также большие количества меди, оказывающие специфическое влияние на форму полярографической волны цинка. Определению цинка мешает также большое содержание в пробе железа и алюминия, с гидроокисями которых заметно соосаждаются ионы цинка как, по-видимому, за счет их сорбции, так и за счет химического взаимодействия ионов цинка с гидроокисями. При этом образуются труднорастворимые соединения типа шпинелей [13], вследствие чего даже многократное переосаждение гидроокисей аммиаком почти не уменьшает потери цинка за счет поглощения его осадком. [43]
Джердил и Лакен [12] измерили полярографические потенциалы полуволн дибензотиофена ( VIII) и его 2 8 -, 3 7 - и 4 6-ди-метилпроизводных в диметилформамиде с помощью ртутного капельного электрода. Потенциалы полуволны восстановления соответственно равны - 2 432; - 2 452; - 2 563 и - 2 501 В отн. Ag AgCl; в тех же условиях гомоароматический аналог флуорен имеет Е г - 2 627 В. Полагают, что во всех случаях процесс включает обратимую одноэлектронную стадию. [44]
Большая часть альдегидов и некоторые кетоны восстанавливаются на ртутно-капельном электроде и могут быть определены полярографически. Потенциалы полуволн восстановления альдегидов менее отрицательны, чем кетонов; присутствие двойной связи в а-положении к карбонильной группе обычно снижает потенциалы восстановления. Такое же влияние оказывает присутствие фенильной группы у ароматических альдегидов и кетонов. [45]
Страницы: 1 2 3 4