Потенциал - разряд
Cтраница 2
Потенциалы разряда ионов железа и кобальта практически равны потенциалу катода. [16]
Величина потенциала разряда через разрядный промежуток составляет 2000 в на каждый его линейный миллиметр. [17]
Величина потенциала разряда через разрядный промежуток составляет 2000 а на каждый его линейный миллиметр. [18]
Величина потенциала разряда через разрядный промежуток составляет 2000 В на каждый его линейный миллиметр. Так как в озонаторе принятого трубчатого типа ширина разрядного промежутка составляет 2 5 мм, то, потенциал разряда будет ир 2 5 2000 5000 В. [19]
Значение потенциалов разряда ионов Cu и Zn2, а также катодный выход металлов по току находятся в зависимости от концентрации в растворе свободного цианида и применяемой катодной плотности тока. С повышением концентрации цианида в растворе концентрация ионов меди уменьшается в большей степени, чем концентрация ионов цинка. Если к тому же учесть, что катодная поляризация более резко выражена при осаждении меди, чем при осаждении цинка, то становится очевидным, что имеется полная возможность управлять процессом совместного осаждения на катоде двух таких отличных в электрохимическом отношении металлов, как медь и цинк. [20]
В интервале потенциалов разряда - ионизации серебра на пастовом электроде не, происходят побочные электродные процессы. [21]
После достижения потенциала разряда адсорбированного реагирующего вещества появляется вторая волна, высота которой при достаточно большой концентрации не зависит от нее. При этом суммарная высота пропорциональна концентрации, так как теперь все продиффундировавшее вещество вступает в реакцию. [22]
Нижним пределом потенциала разряда является потенциал выделения. Потенциалом выделения принято называть такой потенциал, который на бесконечно малую величину превышает равновесный потенциал выделившегося на электроде вещества. [23]
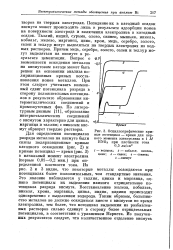 |
Осциллографические кривые потенциал - время для первого момента электролиза в 1 М НМОз при плотности тока 0 5 ма / см2. [24] |
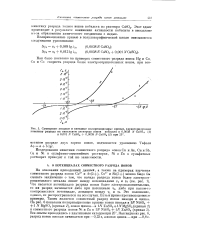
Для определения потенциалов разряда металлов на висмуте были сняты поляризационные кривые катодного осаждения ( рис. 2) и кривые потенциал - время ( рис. 3) в начальный момент электролиза ( первые 0 01 - 0 2 мин. Из рис. 2 и 3 видно, что некоторые металлы осаждаются при потенциалах более положительных, чем стандартные значения. Это явление наблюдается у таллия, цинка и марганца, однако потенциалы их выделения намного отрицательнее потенциала разряда висмута. Восстановление железа, кобальта, никеля, хрома, марганца, цинка, индия, кадмия происходит одновременно с выделением водорода. Таким образом, большинство металлов не должно осаждаться вместе с висмутом во время электролиза, тем более, что потенциал выделения из разбавленных растворов сильно сдвинут в сторону более отрицательных потенциалов, в соответствии с уравнением Нернста. Из полученных результатов следует, что количественное отделение висмута. [25]
 |
Суммарные анодные и катодные поляризационные кривые, характеризующие. [26] |
Что касается потенциалов разряда ионов более электроположительных, то их разряд начинается либо при потенциале PI, либо при каком-то компромиссном потенциале, лежащем между PI и ра. Это положение, однако, не распространяется на все случаи. Есть и прямо противоположные примеры. Таким является совместный разряд ионов никеля и цинка. [27]
Из сравнения потенциалов разряда ионов СЮ и СГ следует, что при совместном присутствии этих ионов в электролите ионы СЮ, даже при незначительной концентрации в растворе, должны были бы значительно легче разряжаться на аноде, чем ионы СГ. [28]
Ввиду близости потенциалов разряда ионов никеля и водорода на катоде во всех случаях наблюдается совместный разряд этих ионов. [29]
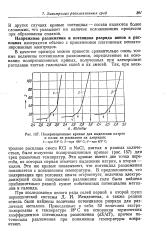 |
Поляризационные кривые для выделения натрия и калия из расплавов их хлоридов. [30] |
Страницы: 1 2 3 4