Потенциал - разряд
Cтраница 4
В растворах четвертичных аммониевых солей потенциал разряда фона сильно сдвигается в отрицательную сторону ( Ек - 2 2 - 2 5 В), увеличиваясь с ростом длины алкильного радикала. Наличие этого фона необходимо, например, при определении таких широко применяемых в синтезе лаковых смол мономеров, как стирол, производные акриловой кислоты, которые восстанавливаются при высоких отрицательных потенциалах. [46]
На рис. 94 показаны зависимости потенциала разряда от плотности тока для двух видов ионов. [47]
Совместное осаждение металлов сопровождается сближением потенциалов разряда их ионов, если на катоде образуется осадок в виде твердого раствора или интерметаллических соединений. В этом случае покрытие образуется при потенциале м енее электроотрицательном, чем потенциал разряда иона менее благородного металла, а иногда и более положительном, чем потенциал разряда ионов более благородного металла, как это наблюдается, например, при осаждении латуни из цианистых растворов солей меди и цинка ( фиг. [48]
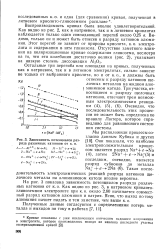 |
Зависимость потенциалов разряда различных катионов от к. о. [49] |
На рис. 3 показана зависимость потенциалов разряда различных катионов от к. Как видно из рис. 3, в натриевом криолито-глиноземном электролите при к. [50]
Этот потенциал очень близок к потенциалу разряда Ка, К или Ва, и волна алюминия не полностью выражена в присутствии больших концентраций указанных ионов. Волна водорода с Е1 / 2 - 1 58 в при рН 3 на фоне 0 007 М раствора 1ЛС1 [377] предшествует и очень близка к волне алюминия. [51]
Этот потенциал очень близок к потенциалу разряда Na, К или Ва, и волна алюминия не полностью выражена в присутствии больших концентраций указанных ионов. LiCl [377] предшествует и очень близка к волне алюминия. [52]
При полярографическом определении катионов с потенциалом разряда отрицательнее - 2 в применяют в качестве фона соли тетраалкиламмония R / J X. [53]
Так как повышение концентрации катионов уменьшает потенциал разряда катиона, то, естественно, из более концентрированных солей осаждение производится при меньшем потенциале, чем из более разбавленных растворов. Так, например, при электролизе 2 % - ного раствора AgNO3 в присутствии Cu ( NO3b медь, обладающая менее электроположительным потенциалом, на катоде не выделяется, если она содержится в небольшом количестве. Однако если концентрация меди достигнет 5 %, то начинается ее совместное выделение с серебром. [54]
Из приведенных данных видно, что потенциалы разряда ионов Сг3 и Сг2 близки к потенциалам цинка, а по величинам перенапряжения водорода хром близок к вольфраму. Трудно себе представить случай, более [ неблагоприятный для электролитического получения металла. [55]
Как видно из этих данных, потенциал разряда фонового электролита в апротонном растворителе - диметилформамиде намного смещен в отрицательную область по сравнению с протогенными. [56]
В соответствии с приведенным уравнением равенство потенциалов разряда ионов нескольких металлов, отличающихся величинами стандартных потенциалов, может быть достигнуто изменением концентрации катионов в электролите и величин перенапряжения их разряда на катоде. [57]
Влияние состава аниона связано с изменением потенциала разряда иона на границе оксид-электролит. Переход к анионам с более низким потенциалом разряда должен действовать как повышение концентрации электролита и соответственно приводить к появлению искрения при меньшей толщине оксидного слоя. [58]
В соответствии с приведенным уравнением равенство потенциалов разряда ионов нескольких металлов может быть достигнуто изменением концентрации катионов в электролите. [59]
Страницы: 1 2 3 4