Потенциал - система
Cтраница 3
Координаты и потенциалы системы общим числом 2 / z называются термодинамическими параметрами состояния. [31]
Ех - потенциал системы ( АОКИсл. [32]
Тем самым потенциал системы адсорбат - адсорбент сводится к потенциалам для адсорбата и адсорбента, взятых в отдельности. В параметры немногих потенциальных функций атом - атом или группа - атом удобно ввести поправки [1], чтобы с помощью этих функций рассчитать термодинамические свойства множества адсорбционных систем. [33]
Так как потенциал системы CeIV / Ceni в точке эквивалентности равен 1 Ю в, потенциал системы VV / V1V - 1 01 в, а потенциал изменения окраски индикатора составляет 1 086 в, то индикаторная ошибка в этом случае очень мала. [34]
Например, потенциал системы цистин - цистеин и ряда других систем снижается при добавлении катализаторов дегидрирования. Добавление к биохимическим системам различных окислительно-восстановительных индикаторов, имеющих одинаковые нормальные потенциалы, нередко приводит к различию в показаниях индифферентных электродов, помещенных в такие растворы. [35]
 |
Формы нахождения сурьмы ( III в растворе в зависимости от рН. [36] |
Нормальный окис лительно-восстановительный потенциал системы Sb / SbH3 в кислой среде равен - 0 50 в, в щелочной - 1 30 а. Эти потенциалы мало отличаются от соответствующих потенциалов мышьяка, од на кг: восстановление Sb в SbH3 происходит значительно медленнее восстановления мышьяка. [37]
Термодинамическое значение потенциала системы СН3ОН / СО2 составляет 0 03 В ( о. [38]
Это разделение потенциала системы на две части будет часто встречаться в дальнейших разделах статьи Максвелла. [39]
Воспользовавшись уравнениями потенциалов систем ( а) и ( б), участвующих в окислительно-восстановительной реакции, можно теоретически решить следующие две задачи: 1) нахождение константы равновесия окислительно-восстановительной реакции и, следовательно, полноты протекания реакции в эквивалентной точке; 2) определение потенциала в эквивалентной точке. [40]
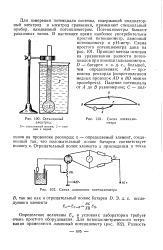 |
Стеклянный электрод.| Схема потенциометра.| Схема лампового потенциометра. [41] |
Для измерения потенциала системы, содержащей индикаторный электрод и электрод сравнения, применяют специальный прибор, называемый потенциометром. Потенциометры бывают различных типов. [42]
Обсудите зависимость потенциала системы Ce ( III) - Ce ( IV) от рН и природы анионов. [43]
Кривые изменения потенциала системы иод-платотетраммин по времени позволяют констатировать резкое падение потенциала, сменяющееся постепенным его изменением. Он может возрастать, уменьшаться или сохранять постоянное значение в зависимости от выбранного молярного отношения реагирующих веществ. [44]
Резкое падение потенциала системы Fe ( II) - Fe ( III) в конечной точке титрования иона Fe3 этилендиаминтетрауксусной кислотой позволяет применять краситель вариаминовый синий В в качестве окислительно-восстановительного индикатора. [45]
Страницы: 1 2 3 4