Потенциал - точка - эквивалентность
Cтраница 1
 |
Кривая титрования хлорида. [1] |
Потенциал точки эквивалентности легко найти по кривой титрования, но и его можно вычислить непосредственно из экспериментальных данных без построения графика. Расчет основан на том, что в точке перегиба кривой вторая производная меняет свой знак и проходит через нуль. Ниже дан пример вычисления первой и второй производной из значений потенциалов электрода, измеренных вблизи точки эквивалентности. [2]
Потенциал точки эквивалентности совпадает с серединой кривой и соответствует ее точке перегиба. Чрезмерная точность определения потенциала точки эквивалентности в данном случае излишняя; небольшие отклонения в ту или другую сторону практически совсем не сказываются на объеме израсходованного рабочего раствора. Если, например, титровать до потенциала Ei или Ez, то это не внесет почти никакой ошибки в определение, так как кривая идет вверх почти совершенно вертикально. [3]
Вычисление потенциала точки эквивалентности основано на использовании констант, характеризующих равновесное состояние между реагирующими веществами. [4]
Зависимость потенциала точки эквивалентности от аналитической концентрации очень слаба, а от рН очень сильна. Изменение рН на единицу меняет потенциал в точке эквивалентности на 0 12 в. Конечно, изменение кислотности и аналитической концентрации бихромата подействует на формальный потенциал пары хром-бихромат, так как доли Cr ( VI) и Cr ( III), связанные в других соединениях ( например, НСгО7, СгО -, СгОН2), изменятся. [5]
В окислительно-восстановительных методах титрования потенциал точки эквивалентности находят из величин нормальных потенциалов окислителя и восстановителя. [6]
В некоторых титраторах при достижении потенциала точки эквивалентности происходит автоматическое отключение бюретки. В данном случае важными становятся как расположение электродов, так и перемешивание раствора, потому что изменение концентрации определяемого вещества вблизи индикаторного электрода должно происходить точно так же, как и в массе раствора. Для проведения титрования используют электронную схему, которая сравнивает фактический потенциал электрода с заранее заданным и отключает бюретку в тот момент, когда эти потенциалы сравниваются. [7]
Доказательство этого математически идентично вычислению потенциала точки эквивалентности в Примере XI. При этом использованы два существенных предположения: в полуреакциях не участвуют ионы Н и раствор окислителя содержит только окисленную форму, а раствор восстановителя - только восстановленную. Если раствор окислителя содержит сколько-нибудь своей восстановленной формы, или наоборот, то потенциал точки эквивалентности несколько смещается. [8]
Для настройки автоматического титрометра необходимо знать потенциал точки эквивалентности, который определяют титрованием вручную. Разность между этой величиной и действительным потенциалом индикаторного электрода усиливают с помощью блока слежения, служащего для контроля скорости подачи титрующего раствора. Следует различать две зоны регулировки: внешнюю зону, далекую от потенциала точки эквивалентности, в которой необходима грубая непрерывная регулировка, и внутреннюю зону с периодической регулировкой. Интервал напряжения внутренней полосы выбирают достаточно узким, чтобы избежать периодического контроля в условиях, когда необходимость в этом отсутствует, но достаточно широким, чтобы предотвратить проскакивание точки эквивалентности. В зоне точки эквивалентности регулировка скорости потока титрующего реагента отсутствует. [9]
Только в том случае, если потенциал точки эквивалентности сохраняется в течение задержки, титрование заканчивается, и тогда на регулирующем устройстве - контроллере загорается предупреждающий сигнал. Титрование урана, которое основано на окислении четырехвалентного урана в шестивалентный ионами трехвалентного железа, генерированными электрохимически [87], следует про водить в растворе, нагретом до 95 1 С. В этом случае регулирующее устройство обеспечивает нагрев и контроль температуры, а также контроль скорости перемешивания. Регулирующее устройство не позволяет начать титрование раньше, чем будет достигнута рабочая температура. [10]
В) не очень сильно отличается от потенциала точки эквивалентности и, как показано в § 4 гл. [11]
 |
Прибор для потенциометрического титрования в инертных растворителях. [12] |
Для точных измерений необходимо, чтобы разность между потенциалом точки эквивалентности и потенциалом полунейтрализации ( потенциал в точке, в которой израсходована половина раствора) составляла 200 - 300 мв / мл. [13]
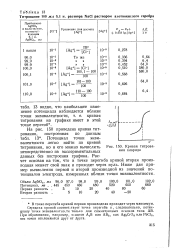 |
Кривая титрования хлорида. [14] |
Середина кривой соответствует точке перегиба и, следовательно, потенциалу точки эквивалентности только для симметричных осадков типа АВ. При образовании, например, осадков А2В или АВа, как Ag2CrO4 илиРЬС12, эти точки отклоняются друг от Друга. [15]
Страницы: 1 2 3 4