Потенциал - электрод - сравнение
Cтраница 3
В графе Титрование без наложения напряжения указаны составы и соответствующие им потенциалы электродов сравнения, рекомендуемых для тех или иных случаев титрования. Приведено лишь несколько простейших систем таких электродов. Если же требуется подобрать электрод с другим значением потенциала, то это можно сделать на основании данных, приведенных в гл. [31]
 |
Прибор типа ППП-58М. [32] |
Электрический потенциал, возникающий на внешней поверхности шарика, сравнивается с потенциалом электрода сравнения, электрически связанным с исследуемым раствором. [33]
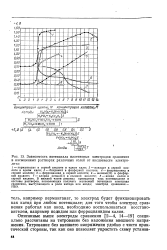 |
Зависимость потенциала платиновых электродов сравнения в насыщенных растворах различных солей от кислотности электролита. [34] |
В нижней части рисунка приводятся ось потенциалов и составы растворов, позволяющих получать желаемый потенциал электрода сравнения, выступающего в роли катода или анода; электрод сравнения - НВЭ. [35]
На практике потенциалом, измеряемым для определения электрического состояния некоторой части электрохимической системы, является потенциал электрода сравнения. [36]
Поскольку в разных сериях опытов возможно изменение в составе промежуточных растворов, лучше использовать эти значения потенциалов электродов сравнения для определения рН ряда хорошо воспроизводимых буферных растворов ( ср. [37]
Контроль этот можно осуществить, фиксируя изменение потенциала катода, на котором происходит выделение металла, относительно неизменного потенциала электрода сравнения. [38]
Используя такую систему, можно представить диаграмму ( рис. 2.11), потенциалы которой сравнены с потенциалом классического электрода сравнения - насыщенного каломельного электрода в водной среде. Следует отметить, что доступные для электрохимических исследований области в органических средах обычно шире, чем в водных. [39]
 |
Макающийся электрод по Ляликову и Кармазину. [40] |
Основным требованием, предъявляемым к электроду сравнения при полярографических и амперометрических определениях, является его неполяризуемость: потенциал электрода сравнения должен оставаться практически постоянным при любой величине наложенного напряжения. Для этого площадь его должна быть неизмеримо больше площади индикаторного электрода. Если площадь электрода сравнения мала, то плотность тока, проходящего в цепи, может оказаться настолько большой, что потенциал электрода изменится - электрод поляризуется. [41]
Наряду с абсолютной величиной диффузионных потенциалов нужно учитывать также и их зависимость от температуры и соответствующую зависимость потенциалов электродов сравнения. При этом для вы - ражения (2.29) важное значение имеет также и зависимость растворимости солей металлов от температуры. По практическим причинам электроды сравнения часто размещают за пределами исследуемой системы при температуре окружающей среды и соединяют со средой солевым мостиком, в котором сглаживаются различия в давлении и температуре. [42]
В отделение электрода сравнения над впаянным в стекло платиновым контактом заливают ртуть и раствор, обеспечивающий постоянство потенциала электрода сравнения. В качестве такого раствора используют насыщенный раствор КС1, растворы НС1, К2 О4, H2SO4 и др. При выборе раствора для отделения электрода сравнения учитывают возможность диффузии компонентов этого раствора в основное отделение и возможность диффузии компонентов анализируемого раствора в отделение электрода сравнения. Поэтому, если, например, в полярографируемом растворе не должны присутствовать хлориды, которые могут препятствовать разрешению пиков определяемого и сопутствующего ЭАВ, то в отделение электрода сравнения не вводят растворы, содержащие хлориды. Если же анализируют растворы, содержащие хлориды, то в отделение электрода сравнения не вводят растворы серной или фосфорной кислоты без хлоридов, так как диффузия хлоридов в это отделение приводит к значительному смещению потенциала электрода сравнения. [43]
Поэтому для измерения потенциала используют электрод сравнения 6, через который поляризующий ток не проходит, а потому потенциал электрода сравнения остается в ходе измерений постоянным. Поскольку в растворе возникает омическое падение потенциала, необходимо измерять потенциал в точке, максимально близко расположенной к поверхности исследуемого электрода. Для этого к поверхности рабочего электрода подводится тонко оттянутая трубочка, которая непосредственно соединена с сосудом электрода сравнения. Внутри этой трубочки, получившей название капилляра Луггина, омического падения потенциала не происходит, так как ток протекает в цепи рабочий электрод - вспомогательный электрод. [44]
Следует отметить, что входящие в уравнения (VI.27) и (VI.28) константы скорости электрохимической стадии k K и k отвечают потенциалу электрода сравнения, от которого отсчитывается соответствующий потенциал полуволны. [45]
Страницы: 1 2 3 4