Стандартный потенциал - металл
Cтраница 2
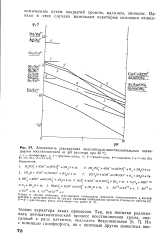 |
Зависимость стандартных окислительно-восстановительных потенциалов восстановителей от рН раствора при 25 С. [16] |
Слева и справа отмечены стандартные потенциалы металлов соответственно в кислой ( рН0) и щелочной ( рН14) средах. [17]
 |
Зависимость стандартных окислительно-восстановительных потенциалов восстановителей от рН раствора при 25 С. [18] |
Слева и справа отмечены стандартные потенциалы металлов соответственно в кислой ( рН 0) и щелочной ( рН 14) средах. Значения потенциалов процессов / - 3 рассчитаны нами, остальные взяты из справочных изданий. [19]
С другой стороны, стандартные потенциалы металлов ( гме) и Других веществ ( например, е) могут быть с известной точностью оценены по изменению изобарных потенциалов ( AZ) соответствующих реакций. [20]
Периодический закон Менделеева и нормальные стандартные потенциалы металлов. [21]
 |
Стандартные электродные потенциалы - в водных растворах. [22] |
Таким образом, таблица стандартных потенциалов металлов является количественным выражением ряда вытеснения металлов. Каждый металл вытесняет из растворов металлы, расположенные ниже его в таблице. Для неметаллов порядок вытеснения обратный: ниже расположенный неметалл вытесняет из раствора выше расположенный. [23]
С увеличением алгебраической величины стандартного потенциала металла уменьшаются восстановительные свойства его атомов и увеличиваются окислительные свойства образующихся при этом катионов. [24]
Таким образом, таблица стандартных потенциалов металлов является количественным выражением ряда вытеснения металлов. Каждый металл вытесняет из растворов металлы, расположенные ниже него в таблице. Для неметаллов порядок вытеснения обратный: ниже расположенный неметалл вытесняет из раствора выше расположенный. Следует помнить, что табличные величины относятся к растворам с а 1; только для таких растворов таблица является рядом вытеснения. Если же берутся растворы иных концентраций, то металлы с близкими по величине ф могут изменить свое относительное положение в ряде вытеснения. Уравнения типа ( XX, 15) и ( XX, 24) позволяют предвидеть это количественно. [25]
Объясните, почему по стандартным потенциалам металлов можно судить, способны они образовывать твердые растворы замещения или нет. [26]
 |
Электродные потенциалы металлов в растворах, и в расплавах хлоридов, в. [27] |
В табл. 9.3 приведены значения стандартных потенциалов металлов в растворах электролитов, измеренных по сравнению с водородным электродом и потенциалов, измеренных в расплавах хлористых молей по сравнению со стеклянно-натриевым электродом. [28]
Гальваностатический метод заключается в измерении стандартных потенциалов металла при пропускании токов заданной плотности, а потенциостатический - в измерении плотности тока при постоянном во времени потенциале. Промышленность выпускает потенциостаты ( П5827, П5827М, П5848), позволяющие проводить комплексные исследования этим методом. [29]
 |
Потенциостати-ческая поляризационная. [30] |
Страницы: 1 2 3 4