Стандартный окислительный потенциал
Cтраница 2
Цель работы состоит в определении кажущегося стандартного окислительного потенциала титруемой системы и титранта, числа электронов, переносимых в каждой системе, константы равновесия оксред-реакции, потенциала в точке эквивалентности и концентрации исходной окисленной или восстановленной формы титруемой системы. [16]
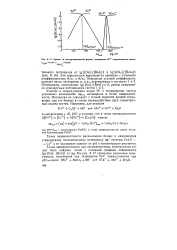 |
Кривая ( в линеаризированной форме титрования Ре2 перманганатом калия. [17] |
Точка эквивалентности расположена ближе к кажущемуся стандартному окислительному потенциалу Дфг системы Сг2С7 - - Сг3 и ее положение зависит от рН и концентрации реагентов. [18]
Электронакцепторную способность редоксита характеризуют с помощью кажущегося стандартного окислительного потенциала, который отражает природу фиксированной в редоксите группы окислительно-восстановительной системы ( рабочего вещества редоксита), взаимное влияние атомов и групп атомов в структуре редоксполимера или взаимное влияние компонентов жидкого редоксита. Выбором рабочего вещества редоксита можно менять кажущийся стандартный окислительный потенциал редоксита, значение которого определяет диапазон его действия. [19]
Приводим пример использования термохимических данных для нахождения стандартного окислительного потенциала [ 142, гл. [20]
Рез концентрационный член может стать равным величине стандартного окислительного потенциала ионов Fe3 или даже превзойти его. Тогда окисление ионов иода ионами трехвалентного железа становится невозможным. [21]
Поскольку окислительный потенциал цинка в щелочной среде значительно меньше стандартного окислительного потенциала водорода при рН 7, цинк восстанавливает водород и в щелочной среде. [22]
Несмотря на важность количественной информации, содержащейся в схемах стандартных окислительных потенциалов, имеется другой, не менее важный аспект в интерпретации результатов оксредметрических измерений. [23]
Американские физико-химики записывают полуреакции как окислительные, сводят в таблицы стандартные окислительные потенциалы, меняя их знаки на обратные при том же численном значении. [24]
Вычислите константу диссоциации для иона тетрамминмеди ( П), используя приведенные ниже стандартные окислительные потенциалы. [25]
Недавно Фрост предложил использовать термин вольт-эквивалент ( ВЭ) для обозначения произведения стандартного окислительного потенциала Е рассматриваемого химического элемента на его степень окисления. [26]
В этом случае целесообразно ввести функцию распределения для окислительно-восстановительных групп по их стандартному окислительному потенциалу. [27]
Ксенон ( VIII) в щелочной среде окисляет иодат до париодата; следовательно, его стандартный окислительный потенциал в щелочном растворе Е0 должен находиться между 0 7 в и потенциалом системы кислород - озон, равным 1 24 в. Мы полагаем, что он ближе к величине 1 24 в, так как, хотя озон осаждает твердый перксе-нонат натрия из раствора Хе ( VI) в 1 М NaOH, в 0 1 М растворе едкого натра Хе ( VI) озоном почти не окисляется. Вполне возможно, что в образовании Хе ( VIII) важную роль играет энергия кристаллической решетки пер-ксеноната натрия. [28]
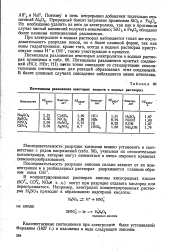 |
Потенциалы разложения некоторых веществ в водных растворах. [29] |
Потенциалы разложения простых соединений ( НС1; HBr; HI) почти точно совпадают со стандартными окислительными потенциалами для реакций образования этих соединений. В более сложных случаях совпадение наблюдается менее отчетливо. [30]
Страницы: 1 2 3 4