Стандартный окислительный потенциал
Cтраница 3
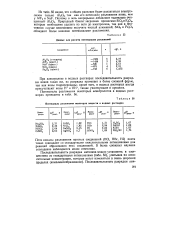 |
Данные для расчета потенциалов разложений.| Потенциалы разложения некоторых веществ в водных растворах. [31] |
Поте нциалы разложения простых соединений ( HCI, HBr, HI) почти точно совпадают со стандартными окислительными потенциалами для реакций образования этих соединений. В более сложных случаях совпадение наблюдается менее отчетливо. [32]
Потенциометрическое определение величины ф основано на проведении в гальваническом элементе окислительно-восстановительной реакции между исследуемой системой с неизвестным стандартным окислительным потенциалом и вспомогательной системой, стандартный окислительный потенциал которой известен. Задача нахождения величины ф системы Ох - Red может быть решена-и в случае, когда такую реакцию в гальваническом элементе провести не удается. [33]
На этих диаграммах стандартную свободную энергию откладывают в зависимости от степени окисления металла таким образом, что стандартный окислительный потенциал для любых двух состояний, образующих пару, равен наклону соединяющей их линии. Чем выше AG для Cu ( I) лежит над линией, соединяющей AG для Си и Си ( II), тем больше разница свободной энергии в пользу реакции диспропорционирова-ния. Подобным же образом восстановление Си ( II) идет в таком случае до свободного металла. Так, наиболее низкая точка на рис. 2 характеризует случай, когда комплекс Си ( II) несколько более устойчив, чем комплекс Cu ( I) ( если судить по разности AG для сольватированных ионов), но когда диспропорционирование Cu ( I) отсутствует. [34]
 |
Схема прибора для измерения окислительного потенциала. [35] |
Если потенциал отнесен к раствору, в котором активности Аокис и Авосст равны единице, говорят о стандартном окислительном потенциале. [36]
 |
Электронные уровни в условиях равновесия на границе полупроводник - раствор электролита. [37] |
На рис. 1.13 приводится несколько вариантов диаграмм распределения энергетических зон на границе полупроводник - раствор в зависимости от стандартного окислительного потенциала редокс-системы и типа полупроводника. [38]
Потенциометрическое определение величины ф основано на проведении в гальваническом элементе окислительно-восстановительной реакции между исследуемой системой с неизвестным стандартным окислительным потенциалом и вспомогательной системой, стандартный окислительный потенциал которой известен. Задача нахождения величины ф системы Ох - Red может быть решена-и в случае, когда такую реакцию в гальваническом элементе провести не удается. [39]
В некоторых случаях, изменяя концентрации ( активности) тех или иных ионов, редокс-реакции можно заставить протекать в направлении, обратном тому, которое соответствует стандартным окислительным потенциалам. [40]
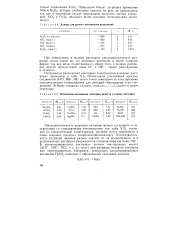 |
Данные для расчета потенциалов разложений.| Потенциалы разложения некоторых веществ в водных растворах. [41] |
Потенциалы разложения некоторых электролитов в водных растворах приведены в табл. 9.5. Потенциалы разложения простых соединений ( НС1, HBr, HI) почти точно совпадают со стандартными окислительными потенциалами для реакций образования этих соединений. В более сложных случаях совпаден с наблюдается менее отчетливо. [42]
Разность потенциалов, которая устанавливается между металлом, погруженным в раствор его соли ( содержащий 1 г-ион металла в литре), и стандартным водородным электродом, называется стандартным окислительным потенциалом металла. Отрицательный потенциал имеют электроды, заряженные отрицательно по отношению к нормальному водородному электроду; во время работы гальванического элемента такой электрод окисляется. Положительный потенциал имеют электроды, которые по отношению к стандартному водородному электроду заряжены положительно; в этом случае во время работы гальванического элемента ионы металла переходят из раствора на электрод. [43]
Наблюдаемое увеличение окислительного потенциала может быть следствием образования в концентрированных растворах уксусной кислоты смешанных сольватокомплексов Fe ( II) и Fe ( III), которые будут характеризоваться другим значением стандартного окислительного потенциала. [44]
Такие стандартные окислительные потенциалы для многих электродных реакций определены экспериментально и содержатся в различных справочниках. [45]
Страницы: 1 2 3 4