Равновесный потенциал - металл
Cтраница 2
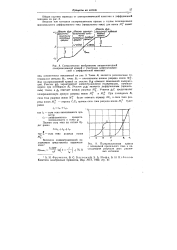 |
Схематическое изображение анодгао-каггодной. [16] |
Точка В является равновесным потенциалом металла Мь точка В3 - потенциалом начала разряда ионов Mj Ход поляризационной кривой на участке B g отвечает химической поляризации. [17]
 |
Диаграмма электрохимической устойчивости воды при 25 С. [18] |
Таким образом, сопоставляя равновесные потенциалы металла и предполагаемого окислителя, можно сделать вывод о вероятности коррозионного процесса. [19]
Еа должен быть положительнее равновесного потенциала металла в данном растворе. То же самое справедливо и по отношению к разряду анионов. [20]
 |
Полная кривая катодной поляризации при электрохимическом восстановлении кислорода. [21] |
Правая часть неравенства (7.35) выражает равновесный потенциал металла в растворе его ионов. [22]
 |
Зависимость потенциалов металлов группы железа от температуры. [23] |
Из таблицы видно, что равновесные потенциалы металлов группы железа при 25 С, полученные на основании экспериментально найденных при высоких температурах величин потенциалов и их температурных коэффициентов, практически совпадают с термодинамически рассчитанными значениями. Стандартные потенциалы никеля, кобальта и железа при этом хорошо согласуются с данными, приводимыми в литературе [9], и составляют соответственно 0 25, 0 27 и 0 44 в ( отн. [24]
Равновесные потенциалы сульфидов намного электроположительнее равновесных потенциалов металлов, поэтому при потенциале металлического анода сульфиды остаются в неизменном виде и переходят в шлам. Количество шлама, в основном, определяется содержанием серы, в анодах - с его увеличением выход шлама резко возрастает. Помимо сульфидов, в шлам переходят содержащиеся в анодах окислы металлов и шлаковые включения. Основная часть металлов группы платины, являясь значительно более электроположительными, чем никель, также остается в шламе. Последний является поэтому коллектором драгоценных металлов. При содержании серы в анодах около 1 % в шлам переходят - от их содержания в анодах - порядка 1 % никеля, кобальта и железа и 5 - 15 % меди. [25]
Положение в ряду напряжений определяется равновесным потенциалом металла в контакте с раствором, содержащим его ионы при концентрации их, равной единице активности. Из двух металлов, составляющих элемент, анодом является более активный металл в ряду напряжений при условии, что активности ионов в равновесии с одним и другим металлом равны единице. [26]
 |
Принципиальная схема работы коррозионного элемента. [27] |
Для более точного суждения необходимо сравнивать равновесные потенциалы металла и водорода при действительно устанавливающихся в растворе активных концентрациях ионов металла и ионов водорода. [28]
Из уравнения (10.10) следует, что равновесный потенциал металла в широких пределах зависит от концентрации ионов металла в растворе. [29]
Чтобы определить заряд поверхности обычно сравнивают равновесный потенциал металла с точкой нулевого заряда. Тогда потенциал р по этой шкале выражается как разность между стационарным потенциалом электрода фст и потенциалом нулевого заряда фн. [30]
Страницы: 1 2 3 4 5