Равновесный потенциал - металл
Cтраница 3
Образование комплексов влияет не только на равновесные потенциалы металлов, но и на величину перенапряжения, и на характер катодных осадков. При переходе от простых электролитов к комплексным обычно наблюдается повышение перенапряжения и уменьшение зернистости осадков; одновременно подавляется тенденция к образованию и росту дендритов. Так, серебро, которое при электролизе раствора его нитрата выделяется на катоде почти без поляризации и дает грубые, шероховатые осадки, может быть получено в виде гладких, тонкокристаллических отложений, если применять комплексные цианистые электролиты. [31]
В связи с этим точное значение равновесного потенциала металлов группы железа очень трудно установить, и точность значений равновесных потенциалов, которые широко используют, весьма относительна. При высоких температурах электролита ( 25 - 250 С), когда плотность тока обмена металла намного превышает плотность тока обмена водорода, определены [8] значения равновесных потенциалов, достаточно близкие к табличным; эти значения потенциала по своей природе соответствуют стационарным. [32]
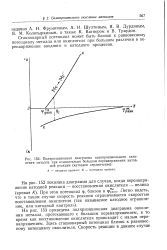 |
Поляризационная диаграмма самопроизвольного окисления металла при относительно большом перенапряжении катодной реакции ( катодное ограничение. [33] |
Стационарный потенциал может быть близок к равновесному потенциалу металла или окислителя при большом различии в перенапряжении анодного и катодного процессов. [34]
Стационарный ( или естественный) потенциал - это равновесный потенциал металла в данном конкретном электролите при отсутствии внешнего тока. При этом потенциале ток, идущий на растворение металла на анодных участках, полностью компенсируется током, идущим на восстановление кислорода на катодных участках. [35]
Как видно, всегда действуют причины, стабилизирующие равновесные потенциалы металла и окислителя. Разумеется все это относится к коррозии в замкнутом или очень медленно сменяемом объеме раствора. В быстром потоке стабилизация равновесных потенциалов затрудняется постоянным удалением продуктов коррозии из слоя, прилегающего к поверхности металла. Но и в этом случае стабилизация возможна, так как приэлектродный слой достаточно малой толщины практически не участвует в движении жидкости. [36]
 |
Схема, иллюстрирующая сущность адсорбционной поляризации. [37] |
Появление комплексов в растворе сказывается не только на равновесных потенциалах металлов, но и на величине перенапряжения и на характере катодных осадков. При переходе от простых электролитов к комплексным обычно наблюдается повышение перенапряжения и уменьшение зернистости осадков; одновременно подавляется тенденция к образованию и росту дендритов. [38]
Появление комплексов в растворе сказывается не только на равновесных потенциалах металлов, но и на величине перенапряжения и на характере катодных осадков. При переходе от простых электролитов к комплексным обычно наблюдается повышение перенапряжения и уменьшение зернистости осадков; одновременно подавляется тенденция к образованию и росту дендритов. Так, серебро, которое при электролизе раствора его нитрата выделяется на катоде почти без поляризации и дает грубые, шероховатые осадки, из комплексных цианистых электролитов может быть получено в виде-гладких тонкокристаллических отложений. [39]
Появление комплексов в растворе сказывается не только на равновесных потенциалах металлов, но и на величине перенапряжения и на характере катодных осадков. При переходе от простых электролитов к комплексным обычно наблюдается повышение перенапряжения и уменьшение зернистости осадков; одновременно подавляется тенденция к образованию и росту дендритов. Так, серебро, которое при электролизе раствора его нитрата выделяется на катоде почти без поляризации и дает грубые, шероховатые осадки, из комплексных цианистых электролитов может быть получено в виде гладких тонкокристаллических отложений. [40]
Водородная деполяризация термодинамически возможна в тех случаях, когда равновесный потенциал металла отрицательнее равновесного потенциала водородного электрода в данных условиях. [41]
Кислородная деполяризация термодинамически возможна в тех случаях, когда равновесный потенциал металла отрицательнее равновесного потенциала кислородного электрода в данных условиях. [42]
Разность потенциалов при динамическом равновесии на границе металл-раствор определяет равновесный потенциал металла или потенциал металл-раствор. Динамическое равновесие металлов, обладающих большей способностью отдавать ионы в раствор, наступает быстрее, чем у металлов, в меньшей степени обладающих этой способностью. Другими словами, равновесие наступает при меньшем равновесном потенциале у металлов с большей способностью отдавать ионы в раствор и, наоборот, при большем равновесном потенциале - у металлов с меньшей способностью. Чем активнее металл, тем большим отрицательным равновесным потенциалом он обладает. Металлы, обладающие малой способностью посылать свои ионы в раствор, могут получать ионы из раствора, тем самым заряжаться положительно и приобретать более положительный равновесный потенциал. [43]
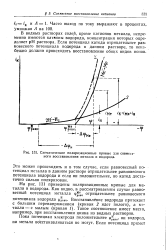 |
Схематические поляризационные кривые для совместного восстановления металла и водорода. [44] |
Это может происходить и в том случае, если равновесный потенциал металла в данном растворе отрицательнее равновесного потенциала водорода и если он положительнее, но катод достаточно сильно поляризован. [45]
Страницы: 1 2 3 4 5