Потеря - протон
Cтраница 3
Движущей силой этого процесса может служить протонирова-ние циклического кислорода остатка рибозы или потеря протона атомом N-1 гетероциклического ядра. [31]
Диазоалканы, как и фосфораны, при ацилировании хлорангидридами дают диазокетоны с потерей протона, отрываемого другой молекулой диазо-алкана. [32]
Изменепие селективности реакции в направлении а связывается с тем 15 ], что потеря протона катион-радикалом определяется в значительной степени стереоэлектроннымн факторами, а не термодинамической стабильностью образующихся свободных радикалов. [34]
Помимо акцепторных свойств катионов диазения, их превращения во многом определяются склонностью к потере протона. Весьма кислыми являются протоны при - углеродных атомах заместителей во фрагменте / N - Nx Особенно легко отщепляется протон от заместителя при втором атоме азота. Например, во всех реакциях, которые могли бы привести к катиону триметилдиазения, получен только диметилгидразон формальдегида. [35]
Начальная стадия может заключаться в реакции амина с двуокисью углерода или ионом бикарбоната с потерей протона. [36]
Например, кетонная и енольная формы пропанона - различные химические соединения, которые при потере протона превращаются в один и тот же мезомерный енолят-анион. [37]
Сила кислоты увеличивается при оттягивании электронов от карбоксильной группы, так как тем самым облегчается потеря протона. Таким образом, сила уксусной кислоты увеличивается при замене атомов водорода атомами галогена. Приводимый ниже ряд кислот характеризует проявление этого эффекта. [38]
Предполагается, что внутримолекулярное алкилирование карбониевого иона другим атомом углерода в голове моста, сопровождающееся потерей протона, ведет к появлению системы с циклопропановым кольцом; алкилирование облегчается пространственной близостью двух участвующих атомов углерода. Играют ли роль протонированные циклопропаны во внутримолекулярном алкилировании или нет, пока не выяснено; однако вполне вероятно, что это алкилирование протекает через протонированный циклопропан с последующей потерей протона и переходом к конечному продукту. [39]
Карбанионы могут быть стабилизованы за счет увеличения вклада 5-электронов в гибридизованную орбиталь, возникающую при потере протона. [40]
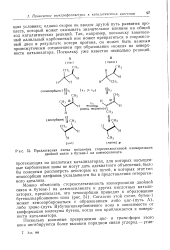 |
Предлагаемая схема механизма стереоселективной изомеризации двойной связи в бутене-1 на алюмосиликате. [41] |
Так, например, поскольку замещенный аллильный карбониевый ион может превратиться в сопряженный диен в результате потери протона, он может быть важным промежуточным соединением при образовании кокса на поверхности катализатора. [42]
Заметим, что мы обсуждаем направление реакции отщепления исходя из понятия переходного состояния, получаемого при потере протона карбониевым ионом, а не переходного состояния в стадии, определяющей скорость реакции и ведущей к образованию карбоние-вого иона. Это объясняется тем, что на состав продуктов реакции влияет как раз стадия, в которой происходит отщепление протона. [43]
Карбанионы могут быть стабилизованы за счет увеличения вклада s - электронов в гибридизованную орбиталь, возникающую при потере протона. [44]
Наиболее интересной особенностью механизма азосочетания является то, что в определенных случаях стадией, определяющей скорость реакции, является потеря протона. Эта особенность обнаруживается двумя способами. Во-первых, при азосочетании некоторых сульфона-фтолят-ионов проявляется первичный изотопный эффект, определяемый, если по месту замещения находится дейтерий, в интервале 4 - 6, и это ясно показывает, что расщепление связи С - Н происходит на стадии, определяющей скорость. Во-вторых, можно показать, что эти реакция азосочетания катализируются основаниями. [45]
Страницы: 1 2 3 4