Потеря - энтропия
Cтраница 1
Потеря энтропии для многих других случаев может быть найдена при помощи этих рассуждений. [1]
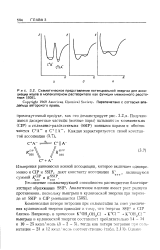 |
Схематическое представление потенциальной энергии для ассоциации ионов в молекулярном растворителе как функции межионного расстояния L505J. [2] |
Компенсация потери энтропии при сольватации за счет увеличения кулоновской энергии приводит к тому, что энергии SS1P и С IP близки. [3]
Требуется определить потерю энтропии в цепи. [4]
Его результатом является потеря энтропии, уменьшающейся тем больше, чем выше заряд. В рассматриваемом случае наблюдается определенная потеря энтропии в исходном состоянии; она является результатом того, что реагирующие частицы имеют заряд. В активированном состоянии уменьшение энтропии должно быть гораздо больше, так как заряд увеличивается. Действительно, при образовании активированного комплекса происходит потеря энтропии. [5]
Помимо вкладов, обусловленных потерями энтропии соответственно при ограничении конформаций всех мономерных единиц, входящих в кольцо, и при первом сшивании цепей, эти величины должны содержать вклады, учитывающие, что при образовании водородной связи после несвязанной пары мономерных единиц изменение свободной энергии не включает в себя членов, обусловленных укладыванием пар оснований друг над другом. Как будет видно из дальнейшего, именно это последнее обстоятельство в основном обусловливает кооперативный характер перехода спираль - клубок в молекулах ДНК. [6]
При образовании циклогексана из этилена потеря энтропии еще больше ( - 86 энтр ед. [7]
При образовании циклогексана из этилена потеря энтропии еще больше ( - 86 энтр. [8]
В то же время А5Ф существенно определяется потерей энтропии в результате фиксации функциональных групп в процессе циклизации в активированном комплексе. [9]
Из табл. 7 видно, что во всех случаях имеется существенная потеря энтропии при низкой величине изменения энтальпии ( а также свободной энергии) в противоположность тому, что было найдено при изучении скорости гидролиза ацеталей. С ростом электроноакцепторной способности re - заместителей величина Kv возрастает. Замена метильных групп в ацетоне на другие приводит к заметному уменьшению Kv, это же имеет место в еще большей степени, если заменить метильную группу на фенил или алкил с разветвлением у а-атома. При замене обеих метильных групп ацетона на циклопропильные остатки образование ацеталя идет нацело. [10]
Нетрудно оценить свободную энергию цепи в полости - другими словами, потерю энтропии от ограничения цени в полости. [11]
Так, при растворении одного иона К и одного иона С1 - потеря энтропии значительно меньше, чем потери при растворении двух атомов аргона, хотя оба иона и-меют электронную конфигурацию атома аргона. [12]
 |
Зависимость - ДС и - е дм разных К ( К1 К2 Лу.| Эксклюзивной хроматографе нейтральных макромолекул ( а и полиэлектролитов. иовнш эксклюзш ( в, ионообменная сорбция (. [13] |
Гиббса не изменяется ( - ДО 0), происходит полная компенсация потери энтропии макромолекулы благодаря увеличению энтальпии: - АН - ТАЗ, т.е. переход макромолекулы из р-ра в поры энергетически безразличен. При - ДО0 и Кл 1 наблюдается адсорбционная хроматография. [14]
На внутреннее вращение неполярных боковых цепей влияют несколько факторов, которые уменьшают потерю энтропии до значений, намного меньших, чем 5 э.е. Рассчитанные Немети и Шерага значения А. [15]
Страницы: 1 2 3 4