Потеря - энтропия
Cтраница 2
Поэтому ( в условиях такой компенсации потенциальной свободной энергии сорбции и сопровождающих сорбцию потерей энтропии) может оказаться, что наблюдаемые значения АО, отражающие суммарный эффект ( уравнение 2.31), примут для обеих моделей примерно одинаковые значения. Эти модели, однако, должны отличаться по свободной энергии активации последующего химического взаимодействия X Y, протекающего в фермент-субстратном комплексе. [16]
 |
Газы на кристаллах ( стандартное состояние 0 i / 3. [17] |
В этот раздел входит большинство веществ, адсорбирующихся физически; только в исключительных случаях потерю энтропии можно приписать потере целых степеней свободы. [18]
 |
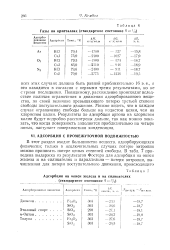
Энтропии полимеризации и адсорбции В А и ММА на поверхности и в жидкой фазе ( значение энтропии мономеров в газовой фазе условно принято за 0. М и П - мономер и полимер. [19] |
Это может быть соотнесено с соответствующим уменьшением энтропии адсорбированных мономеров при образовании АК, причем потеря энтропии для ВА оказывается существенно большей, чем для ММА. Этот результат согласуется с адсорбционными данными, приведенными в разд. [20]
Ответ состоит в том, что включение сопряженного основания в переходное состояние скомпенсирует связанную с этим потерю энтропии. Если сопряженное основание является анионом А -, а остальная часть переходного состояния несет положительный заряд, то электростатическое взаимодействие может скомпенсировать потерю поступательной и вращательной энтропии. [21]
Как видно, свободная энергия переноса молекулы реагента из воды в мицеллярную фазу может практически полностью компенсировать предполагаемую потерю энтропии при включении молекулы общеосновного или общекислотного катализатора в переходное состояние реакции. Эта компенсация и обусловливает некоторое подобие механизмов ферментативного и мицеллярного катализа. В отличие от реакций высокого кинетического порядка, протекающих в результате взаимодействия низкомолекулярных реагентов непосредственно в растворе, в том и другом случае катализа почти отсутствует неблагоприятный инкремент свободной энергии активации, связанный с потерей поступательного и вращательного движений при включении в переходное состояние реакции дополнительной частицы. Разумеется, конкретный механизм этого явления в каждом из видов катализа несколько иной. В мицеллярном катализе имеет место рассмотренная выше компенсация энтропийных потерь за счет свободной энергии термодинамически выгодных ионных и гидрофобных взаимодействий реагента с мицеллой. [22]
По мнению Г.А. Крестова [14], физический смысл величины AS в состоит в том, что она характеризует потерю поступательной составляющей энтропии рассматриваемой частицы при ее переходе из газообразного состояния в раствор. [23]
Этот результат показывает, что при распространенном в практике выборе полосы пропускания по ослаблению на границах - , потеря энтропии не превышает - 0 2 дв. [24]
Низкие частотные факторы для реакций присоединения Дильса - Альдера, приведенные в табл. XII.8, можно объяснить с точки зрения значительной некомпенсированной потери вращательной энтропии при образовании критического комплекса. [25]
Низкие частотные факторы для реакций присоединения Дильса - Альдера, приведенные в табл. XI 1.8, можно объяснить с точки зрения значительной некомпенсированной потери вращательной энтропии при образовании критического комплекса. [26]
В частности, линейно возрастающее усиление С ( со) со или пилообразная характеристика между 0 и 1 имеют такую же потерю энтропии. [27]
Второй член описывает контактные взаимодействия с поверхностью: Тб есть эффектное притяжение, испытываемое адсорбированным на поверхности мономером; оно определяется конкуренцией между энергией притяжения и потерей энтропии, / ь - доля связанных мономеров. [28]
Второй член описывает контактные взаимодействия с поверхностью: Тб есть эффектное притяжение, испытываемое адсорбированным на поверхности мономером; оно определяется конкуренцией между энергией притяжения и потерей энтропии, /, - доля связанных мономеров. [29]
Недавно, например, была высказана гипотеза [134], что энтропии гидратации вообще не содержат вклада от влияния растворенной молекулы на воду, но определяются исключительно потерями энтропии самой растворенной молекулой при переносе ее из газовой фазы в раствор. Автор [134] даже предположил, что в данном растворителе любая молекула теряет одинаковую долю газофазной энтропии, а именно: такую, которая характеризует перенос газ - - жидкость молекулы самого растворителя. [30]
Страницы: 1 2 3 4