Потеря - энтропия
Cтраница 3
 |
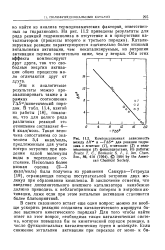
Изменение величин ДЯ и Т Д5 под влиянием различных типов катализаторов. [31] |
Кроме того, в некоторой степени уменьшается и свобода вращения, поскольку обе молекулы должны точно сохранять надлежащую взаимную ориентацию. Потеря энтропии при катализе ферментами компенсируется дополнительным понижением энтальпии, причина которого - связывание с образованием комплекса. [32]
Его результатом является потеря энтропии, уменьшающейся тем больше, чем выше заряд. В рассматриваемом случае наблюдается определенная потеря энтропии в исходном состоянии; она является результатом того, что реагирующие частицы имеют заряд. В активированном состоянии уменьшение энтропии должно быть гораздо больше, так как заряд увеличивается. Действительно, при образовании активированного комплекса происходит потеря энтропии. [33]
Более интересным является величина потери энтропии на цепи вычислительных шагов, которая равна произведению величины р на это число шагов. [34]
Поэтому при образовании активированного комплекса потеря энтропии не так велика, как для неполярных растворителей, т.е. растворителей со слабыми акцепторными свойствами, молекулы которых лишь незначительно взаимодействуют друг с другом. [35]
В ходе бимолекулярной реакции вида А В при переходе ют основного к переходному состоянию теряется значительная часть поступательной и вращательной энтропии. Однако если процесс включает образование комплекса и последующую внутримолекулярную реакцию, то неблагоприятная потеря энтропии происходит уже ( по крайней мере частично) в основном состоянии, так как реагенты ( одним из них может быть катализатор) в ходе комплексообразования теряют поступательную вращательную энтропию. [36]
Экстраполяция этой линии для других заместителей определяет вклад пути ks для них. Отметим, что увеличение скорости при переходе к электронодонорным заместителям обусловлено уменьшением потери энтропии в процессе активации; энтальпия активации при этом несколько увеличивается. [37]
В табл. 11.4, взятой из работы [18], показано, что для целого ряда различных реакций это отношение составляет 4 - 6 ккал / моль. Такая величина сопоставима со значением 5 4 ккал / моль, предложенным для учета потери энтропии при введении одной молекулы воды в переходное состояние. [39]
Ответ состоит в том, что включение сопряженного основания в переходное состояние скомпенсирует связанную с этим потерю энтропии. Если сопряженное основание является анионом А -, а остальная часть переходного состояния несет положительный заряд, то электростатическое взаимодействие может скомпенсировать потерю поступательной и вращательной энтропии. [40]
Если j предшествующих пар оснований не связаны, то образование водородной связи в ( / -) - 1) - й паре приводит к образованию кольца цепи из j пар несвязанных оснований, что накладывает некоторые ограничения на конформации всех мономерных единиц, входящих в кольцо; соответствующее изменение свободной энергии может быть включено в свободную энергию образования водородной связи в ( y - f - 1) - й паре оснований. Наконец, если все мономерные единицы, предшествующие рассматриваемой паре оснований, не связаны, то изменение свободной энергии при образовании водородной связи должно включать в себя потерю энтропии при появлении первой сшивки между двумя цепями. [41]
Приемлемое объяснение состоит в том, что эффект сопряжения ( М) первоначального заместителя хлора стабилизует электронодефицитный центр радикала в радикал-аддукте в большей степени, чем исходный олефин. В результате прямая реакция первой стадии оказывается не только более экзотермичной, чем в реакции этилена, но также обусловливает отрицательный инкремент в ее свободной энергии, несмотря на потерю трансляционной энтропии. Таким образом, вместо самопроизвольного распада радикал-аддукт должен разрушать молекулу хлора. Кинетическое уравнение также показывает, что обрыв цепи проходит с участием двух хлоралкильных радикалов, которые, вероятно, либо коллигируются, либо диспропорционируют. Кинетические цепи имеют достаточно большую длину. [42]
Реакционный комплекс иногда называют комплексом столкновения, однако совершенно очевидно, что простого столкновения далеко недостаточно для образования структуры, в которой возможен перенос протона. Работа Wr, которую необходимо затратить для образования реакционного комплекса, представляет собой по существу ту часть AF HA, которая не зависит от изменений р / СанА - Величина Wr, необходимая для переноса протона с членов гомологического ряда кислородных кислот на один и тот же субстрат, согласно предположению, определяется потерями энтропии при фиксации молекулы кислоты и свободной энергией ее десольватации. Свободная энергия десольватации третичных аминов практически не коррелирует с их основностью. Сольватация аминов обусловлена главным образом ван-дерваальсовскими взаимодействиями, которые играют заметную роль и при сольватации ионов, поэтому разумно предположить, что свободная энергия десольватации аммониевых солей также никак не связана с их кислотными свойствами. Было показано, что даже прочность водородных связей лишь слабо коррелирует с силой кислот. [43]
Стиллинджер пришел к выводу, что молекулы воды, прилегающие к полости, ориентируются так, что три их фундаментальных тетраэдрических направления как бы охватывают полость, а четвертое направлено радиально наружу. Пара таких молекул воды образует связь в заслоненной конфигурации. Эти геометрические ограничения термодинамически должны приводить к потере энтропии, что и проявляется в отрицательных энтропиях растворения. [44]
Уменьшение силы кислот при переходе от щавелевой кислоты к азелаиновой ( за исключением янтарной кислоты) снова может быть объяснено в основном действием энтропийного эффекта. По-видимому, в случае низших кислот ( щавелевой, малоновой) проявляются какие-то стерические затруднения, связанные с близостью отрицательных зарядов, уменьшающих электро-стрикцию молекул воды. С увеличением расстояния между зарядами по мере перехода к высшим членам ряда потери энтропии при диссоциации возрастают. [45]
Страницы: 1 2 3 4