Нуклеофильный заместитель
Cтраница 3
Рассмотрим теперь избирательность, зависящую от различной скорости разрушения ФОС. Разрушением можно считать любую реакцию, которая делает атом фосфора менее электроположительным; обычно это происходит за счет введения более нуклеофильных заместителей. В известных нам случаях ( малатион, ацетион) образуется анион за счет гидролиза карбоксиэфирной связи. Сюда же можно отнести гидролиз карбоксиамидной связи, как это происходит при разрушении диметоата ( стр. Разумеется, наиболее универсальным является гидролиз фосфатноэфирной связи ФОС. [31]
Более того, последние исследования ( как показано выше и в гл. RO) ( НО) Р ( О) ОХ и что в некоторых случаях может иметь место циклизация, если нуклеофильный заместитель - анион или, возможно, третичный азот - расположены соответствующим образом. [32]
Такими центрами могут быть карбониевые ионы или карбанионы. Там, где выбор невозможен, как в случае различных виниловых соединений, возможно [4], что мономеры с электрофильными заместителями полимеризуются по свободнорадикальному или карба-нионному механизму, а мономеры с нуклеофильными заместителями - через карбониевый ион ( см. стр. Так, реакции ионной полимеризации, вероятно, имеют более низкие энергии активации развития цепи, хотя они имеют также и более низкие предэкспоненциальные множители. Константы скоростей отдельных стадий ионной полимеризации не измерялись, но, как показывают данные табл. 42, общая энергия активации для многих реакций катионной полимеризации очень мала. Имелись сообщения об отрицательных величинах энергии активации, что резко отличается от свободнорадикальных реакций полимеризации. Кроме того, наблюдается большее разнообразие законов скорости. [33]
Количественным выражением основности аминов служат их константы ионизации, определяемые обычно методом потенциометри-ческого титрования. Нуклеофильные заместители, затрудняя сопряжение неподеленной пары с ядром, повышают основность аминов, электро-фильные благоприятствуют ее сопряжению с ядром и понижают основность аминов. [34]
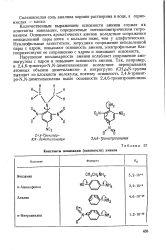 |
Константы ионизации ( основности аминов. [35] |
Количественным выражением основности аминов служат их константы ионизации, определяемые потенциометрическим титрованием. Нуклеофильные заместители, затрудняя сопряжение неподеленной пары с ядром, повышают основность аминов, электрофильные благоприятствуют ее сопряжению с ядром и понижают основность. [36]
Рассмотрим это на хорошо изученном процессе восстановления активных групп у замещенных бензола. Электрофяльные заместители, проявляющие - / - или - С-эффект, вызывая оттягивание электронов, уменьшают электронную плотность на активной группе и облегчают ее восстановление. Нуклеофильные заместители, проявляющие / - или С-эффект, повышая электронную плотность на активной группе, затрудняют восстановление этой группы. [37]
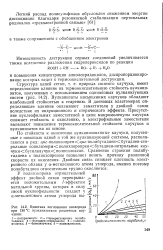 |
Кинетика поглощения кислорода при 130 С вулканизатами различных каучуков. [38] |
Вулканизаты насыщенных каучуков обладают наибольшей стойкостью к старению. В диеновых эластомерах определяющее влияние оказывают заместители у двойной связи вследствие их индукционного и стерического эффекта. Присутствие нуклеофильных заместителей в цепи макромолекулы каучука снижает стойкость к окислению, а электрофильные заместители вызывают повышение термоокислительной стойкости каучуков и вулканизатов на их основе. [39]
Структура изоцианатов существенно влияет на скорость реакции. Если в бензольном кольце есть электрофильные заместители, то скорость реакции возрастает. Наоборот, нуклеофильные заместители, особенно в орто-положении, снижают скорость реакции. [40]
При реакции комбинирования между нитрильными лигандами и алкиль-ными группами ( галоидалкилами) образуются изонитрильные лиганды. Реакция комбинирования арильных лигандов ( из арилиодидов) с лигандами ( RC С) приводит к диарилацетиленам. Если арилиодид в орто-поло-жении имеет нуклеофильный заместитель, продуктом реакции является гетероциклическое соединение типа 3-фенилизокумарина, 2-фенилбензофурана и замещенных индолов. [41]
Для цинка ингибирующий эффект ароматических аминов в зависимости от констант Гаммета прямо противоположен тому, который наблюдался для железа и никеля. Объясняется это тем, что при наличии отрицательного заряда ( срст-срн. В) уменьшение электронной плотности на адсорбционном центре молекулы, которое происходит при введении нуклеофильных заместителей, должно способствовать электростатической адсорбции и увеличивать ингибирующий эффект. Что же касается специфической адсорбции, то для цинка она не характерна. [42]
Когда невозможно провести реакцию в газовой фазе, используют инертные растворители, например к-гексан и мезитилен. В этих растворителях реакции становятся реакциями второго порядка по концентрации L. Это предполагает, что растворитель действительно играет активную роль, и в случае некоординирующегося растворителя нуклеофильный заместитель обязательно участвует в реакции. [43]
 |
Относительная реакционная способность. [44] |
Рассмотрение тонких деталей механизма и противоречивых точек зрения по этому вопросу выходят за пределы данного раздела. Однако следует отметить, что в процессе замещения галогена могут участвовать соседние группы или атомы X, которые находятся в подходящем для этого положении [ схема ( 85) ]; при этом в действительности весь процесс замещения включает две 5лг2 - подоб-ных реакции, что приводит в результате к сохранению конфигурации. При протекании реакции по такой схеме преимущество подобного пути по сравнению с прямым замещением Y - состоит в меньшем изменении энтропии при внутримолекулярном процессе. Соучаствующая группа может быть подходящим нуклеофильным заместителем, таким как ОН, SH, NH, Hal или СООН. В ходе реакции могут образовываться циклические интермедиаты с различным размером цикла. Кроме того, X может представлять собой я-электронную систему двойной связи или ароматического кольца или же, что более спорно [72, 73], это может быть а-электронная система, которая, например в случае циклопропильных или норбор-нильных заместителей, может участвовать в реакции аналогично я-системе. [45]
Страницы: 1 2 3 4