Электроно-акцепторный заместитель
Cтраница 3
Данные Розенблюма [6] по ацилированию фенилферроцена подтверждают наши результаты: фенильная группа, подобно другим электроно-акцепторным заместителям, оказывает дезактивирующее влияние на электрофильное замещение водородов ферроценового ядра. [31]
Все точки в соответствии с последним уравнением хорошо ложатся на корреляционную прямую, за исключением электроно-акцепторных заместителей. Это обусловлено наличием прямого полярного сопряжения заместителя с атомом фтора, проявляющим - J - С-эффект. [32]
 |
Зависимость lgA0TH / ( ( I. [33] |
Как видно из приведенных данных, природа заместителя X существенно влияет на скорость симметризации, причем электроно-акцепторные заместители ( NO2, Hal) ускоряют, а электронодонорные ( Alk) тормозят реакцию. При X NO2 реакция идет настолько быстро, что не удается измерить ее скорость. [34]
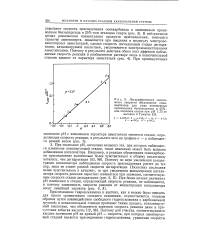 |
Логарифмическая зависимость скорости образования семи-карбазона для ряда замещенных производных бензальдегида в 25 % - ном этиловом спирте при рН 1 75 от величин ст Гаммета. [35] |
В нейтральных средах равновесная концентрация продукта присоединения, имеющего характер аминоспирта, повышается при введении в молекулу электроно-акцепторных заместителей, однако скорость последующей стадии дегидратации, катализируемой кислотами, увеличивается электроноакцепторными заместителями. [36]
К по способности комплексов экстрагировать ионы К и Na Величины К комплексов Na с производными краун-эфиров, содержащими электроно-акцепторные заместители, были больше, чем соответствующие константы их комплексов с К, тогда как для 18-членных краун-эфиров наблюдалось обратное соотношение. [37]
Выводы эти согласуются с нашим давнишним качественным выводом о том, что одно из отличий ферроценовой системы от бензола в том, что последний одинаково податлив к действию электронодонорных и электроно-акцепторных заместителей, в то время как ферроцен податлив только к требованиям электроноакцепторов. Обычными путями: 1) гидролизом фер-роценилметилтриалкиламмония [328] и 2) используя действие литий - и магнийорганических соединений на кетоны и нитрилы ферроценового ряда, мы получили ферроценил - [331, 332] и триферроценил [333] карбинолы и соответственные карбониевые соли. [38]
Если пиррол очень активен по отношению к электрофильным реагентам, то при введении в него атома азота пиридинового типа доступность электронов снижается, и азолы реагируют с электрофилами подобно пирролам с одним или более электроно-акцепторными заместителями в кольце. [39]
Квантово-химические расчеты с сопоставлением потенциалов ионизации производных бензола и молекулы N02 показывают, что для нитрования толуола и ксилола катионом нитрония NOa 1 более вероятей путь через ион-радикальную пару, для нитробензола и других производных с электроно-акцепторными заместителями - только классический полярный механизм, а для бензола - как тот, так и другой [288], Аргументами в пользу механизма с переносом электрона являются согласованность изменений активности ( ароматических соединений и их потенциалов ионизации, соответствие ориентации замещения с распределением спиновой плотности в катион-радикалах, экспериментально показанная возможность генерирования катион-радикалов в условиях, близких к условиям реакции замещения. Эти аргументы касаются обоснования вероятности акта переноса электрона, но не могут служить доказательством того, что он действительно реализуется и, главное, что он лежит на координате реакции. Поэтому особое значение приобретают поиски прямых экспериментальных свидетельств ион-радикального механизма. [40]
При реакции с более кислыми веществами и особенно при кислотном катализе реакционная способность изменяется в обратном направлении и образуется значительное количество аномального изомера ( II), что в еще большей мере относится к а-оксидам, имеющим электроно-акцепторные заместители. [41]
Современная электронная теория цветности основана на работах В. А. Измаильского, начатых им в 1915 г. В. А. Измаильский объяснял цветность органических соединений особым электронным состоянием молекул, имеющих на одном конце длинной цепочки сопряженных двойных связей электронодонорные, а на другом - электроно-акцепторные заместители. [42]
Вследствие небольшой активности ионов диазония реакция протекает направленно с образованием п - или о-изомеров. Электроно-акцепторные заместители в диазониевом ионе повышают его реакционную способность, а электронодонорные группы понижают ее. [43]
Таким образом, константы Гаммета характеризуют величину и знак заряда, который создает заместитель ( в результате индуктивного и ме-зомерного эффектов) у узлового атома бензольного кольца. Электроно-акцепторные заместители, характеризующиеся положительной величиной константы а, создают положительный заряд у узлового атома, элек-тронодонорные заместители с отрицательной величиной а создают отрицательный ( или снижают положительный) заряд у узлового атома. [44]
У замещенных в ядре производных бензоилпероксида наиболее существенное изменение инициирующей активности достигается введением заместителей в орто-положение [ 31, с. Электроно-акцепторные заместители снижают активность пероксида, электро-нодонорные - повышают ее. Влияние некоторых заместителей может быть весьма специфичным [ 43, гл. [45]
Страницы: 1 2 3 4