Метильный заместитель
Cтраница 2
Цифры показывают положение метильных заместителей. [16]
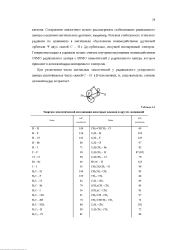 |
Энергии гемолитической диссоциации некоторых алканов и других соединений. [17] |
При увеличении числа метильных заместителей у радикального углеродного центра увеличивается число связей С - Н в ( 3-положениях, и, следовательно, степень делокализапии возрастает. [18]
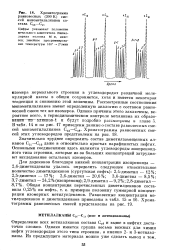 |
Хроматограмма равновесных ( 300 К смесей монометилалканов состава С13 - С18. [19] |
Цифры указывают положение метильного заместителя. [20]
Подобным образом n - метильный заместитель стабилизирует образующийся радикал и, следовательно, стабилизирует переходное состояние в той степени, в какой оно сходно с продуктом. [21]
Известно, что наличие метильных заместителей снижает эффективность этих соединений как антиоксидантов. Наблюдается небольшая разница в константах скоростей между о - и и-бисфено-лами ( № 30 и 34), причем в отличие от монофенолов более реак-ционноспособным оказался о-бисфенол. Возможным объяснением этого факта является уменьшение стерических затруднений у о-соединения по сравнению с га-бисфенолом. [22]
В реакции 2 4-толуилендиизоцианата с бутанб-лом метильный заместитель дезактивирует изоцианатную группу, повышая ее электроотрицательность, причем этот эффект сильнее в том случае, когда заместитель находится в орто-положении к ней. Одна изоцианатная группа повышает активность другой за счет электронооттягивающего эффекта. [23]
В этом синтезе переход от метильного заместителя к пропильному реализуется через литийорганическое соединение. Далее получают оксид, обрабатывают его РОСЬ и хлорпроизводное переводят в нитрил действием NaCN. Обработкой сероводородом нитрил переводят в тиоамид. [24]
Начало нумерации определяется старшинством двух метильных заместителей против одного и старшинством метилацидной группы против метильной. [25]
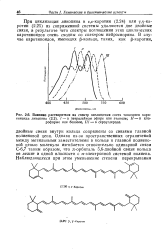 |
Влияние растворителя на спектр поглощения света типичного каро-тииоида ликопииа. / - в петролейиом эфире или этаноле. / / - в хлороформе или бензоле, / / / - в сероуглероде. [26] |
Однако из-за пространственных ограничений между метильными заместителями в кольце и главной полиеновой цепью молекула изгибается относительно одинарной связи С-67 таким образом, что я-орбиталь 5 6-двойной связи кольца не лежит в одной плоскости с я-электронной системой полиена. [27]
Из этих данных видно, что метильный заместитель дезактивирует изоцианатную группу, повышая ее электроноотрицатель-ность, причем этот эффект сильнее, когда заместитель находится в о / даго-положении к ней. Одна изоцианатная группа повышает активность другой за счет электронооттягивающего эффекта, что видно из большей реакционной способности диизоцианатов по сравнению с моноизоцианатом. Из таблицы также видно, что после того, как первая изоцианатная группа прореагировала, реакционная способность второй функциональной группы снижается примерно на целый порядок, что обусловлено значительно меньшей электронооттягивающеи способностью уретановои группы по сравнению с изоцианатной. [28]
Из приведенной структуры видно, что метильные заместители находятся достаточно близко к атому металла, чтобы вызвать пространственные затруднения атаке других лигандов вдоль оси октаэдра и препятствовать перегруппировке молекулы в конфигурацию с тетраэдрическим расположением лигандов. Плоскости мезитильных колец перпендикулярны координационной плоскости кобальта, но расположены не вполне симметрично относительно этой плоскости. [29]
Однако известны определенные благоприятствующие положения для метильных заместителей. Для нескольких рядов алкилпроизводных 1 2-бензантрацена установлено, что канцерогенная активность уменьшается при удлинении углеродной цепи. При введении многих других заместителей получены канцерогенные соединения, приче. [30]
Страницы: 1 2 3 4