Принцип - наименьшая энергия
Cтраница 1
 |
Энергетическая диаграмма распределения электронов по орбита-лям для 25-го элемента ( 25Мп. [1] |
Принцип наименьшей энергии - для получения электронной конфигурации основного состояния атома или иона необходимо заполнять электронами свободные орбитали с наименьшей энергией. [2]
Принцип наименьшей энергии справедлив только для основных состояний атомов. В возбужденных состояниях электроны могут находиться на любых орбиталях атомов, если при этом не нарушается принцип Паули. [3]
Принцип наименьшей энергии и правило Гунда справедливы только для основных состояний атомов. В возбужденных состояниях электроны могут находиться на любых орбиталях атомов, если при этом не нарушается принцип Паули. [4]
Поэтому принцип наименьшей энергии определяет порядок заполнения энергетических подуровней: электроны заполняют энергетические подуровни в порядке увеличения их энергии. [5]
Почему принцип наименьшей энергии определяет порядок заполнения энергетических подуровней. [6]
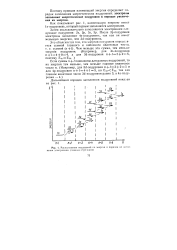 |
Расположение подуровней по энергии и порядок их заполнения электронами ( показан стрелками. [7] |
Поэтому принцип наименьшей энергии определяет го-рядок заполнения энергетических подуровней: электроны заполняют энергетические подуровни в порядке увеличения их энергии. [8]
Почему принцип наименьшей энергии определяет порядок заполнения энергетических подуровней. [9]
Согласно принципу наименьшей энергии и принципу Паули эти два электрона с противоположными спинами также заселяют оу-орбиталь. [10]
Согласно принципу наименьшей энергии и принципу Паули, эти два электрона с противоположными спинами также заселяют сгсв15 - орбиталь. [11]
 |
Энергетическая диаграмма уровней атомных и молекулярных орбиталей. [12] |
Согласно принципу наименьшей энергии и принципу Паули эти два электрона с противоположными спинами также заселяют асв1 - орбиталь. [13]
Согласно принципу наименьшей энергии и принципу Паули, эти два электрона с противоположными спинами также заселяют тсв. [14]
Как формулируется принцип наименьшей энергии. [15]
Страницы: 1 2 3 4