Принцип - наименьшая энергия
Cтраница 2
Это отвечает принципу наименьшей энергии. [16]
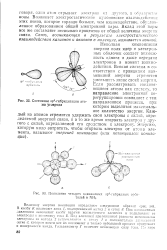 |
Состояние р3 - гибридизации это ма углерода.| Появление четырех одинаковых 5р3 - гибридных орби-талей в МНз. [17] |
Всякая система в соответствии с принципом наименьшей энергии стремится уменьшить запас своей энергии. [18]
 |
Примеры связей различной симметрии. а - ст-связи. 6 - л-связи. [19] |
Возникшие МО заполняются электронами в соответствии с принципами наименьшей энергии, а также принципами Паули и Хунда аналогично заполнению электронных орбиталей атома. [20]
Заполнение электронных уровней осуществляется в соответствии с принципом наименьшей энергии: наиболее устойчивому состоянию электрона в атоме отвечает состояние с минимальным значением энергии. Поэтому вначале заполняются слои с наименьшими значениями энергии. Клечковский установил, что энергия электрона возрастает по мере увеличения суммы главного и орбитального квантовых чисел ( п /), поэтому заполнение электронных слоев происходит в порядке увеличения суммы главного и орбитального квантовых чисел. [21]
 |
Схема заселенности МО молекул, образованных атомами элементов первого периода. [22] |
В основном состоянии молекулы два ее электрона согласно принципу наименьшей энергии занимают наиболее низкую орбиталь crls и согласно запрету Паули имеют противоположные спины. Оба электрона занимают четную ( g) орбиталь. По правилу произведения ( g x g g состояние системы четное. [23]
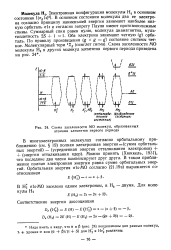 |
Схема заселенности МО молекул, образованных атомами элементов первого периода. [24] |
В основном состоянии молекулы два ее электрона согласно принципу наименьшей энергии занимают наиболее низкую орбиталь als и согласно запрету Паули имеют противоположные спины. Оба электрона занимают четную ( g) орбиталь. По правилу произведения ( g x g g) состояние системы четное. [25]
Распределение электронов в атоме осуществляется в соответствии с принципом наименьшей энергии. Это значит, что и энергия их в этом положении меньше. [26]
Распределение электронов в атоме осуществляется в соответствии с принципом наименьшей энергии. [27]
Освещая тему о строении многоэлектронных атомов, рассказать о принципах наименьшей энергии, Паули, правиле Гунда, привести полную электронную формулу элемента 105, составленную на основании этих принципов, указать, как пользоваться этой формулой для конкретных элементов. [28]
При заполнении электронных слоев и оболочек атомы подчиняются: 1) принципу наименьшей энергии, согласно которому электроны сначала заполняют вакантные орбитали с минимальной энергией; 2) принципу Паули; 3) правилу Гунда - на вырожденных орбиталях суммарное спиновое число электронов должно быть максимальным. В квантовых ячейках с одинаковой энергией заселение электронами происходит так, чтобы атом имел наибольшее число неспаренных электронов. У каждого следующего элемента Периодической системы по сравнению с предыдущим на один электрон больше. Наиболее прост первый период системы, состоящий лишь из двух элементов. У водорода единственный электрон заселяет наинизшую по энергии орбиталь Is, а у гелия на этой орбитали два электрона с антипараллельными спинами. Таким образом, у атома гелия полностью формируется наиболее близкий к ядру Ал-слой. [29]
При заполнении электронных слоев и оболочек атомы подчиняются: 1) принципу наименьшей энергии, согласно которому электроны сначала заполняют вакантные орбитали с минимальной энергией; 2) принципу Паули; 3) правилу Гунда - на вырожденных орбиталях суммарное спиновое число электронов должно быть максимальным. В квантовых ячейках с одинаковой энергией заселение электронами происходит так, чтобы атом имел наибольшее число неспаренных электронов. У каждого следующего элемента Периодической системы по сравнению с предыдущим на один электрон больше. Наиболее прост первый период системы, состоящий лишь из двух элементов. У водорода единственный электрон заселяет наинизшую по энергии орбиталь Is, а у гелия на этой орбитали два электрона с антипараллельными спинами. Таким образом, у атома гелия полностью формируется наиболее близкий к ядру К-слой. [30]
Страницы: 1 2 3 4