Природа - аминокислота
Cтраница 3
Согласно позднейшим исследованиям223, наблюдаемое окрашивание присуще не какому-то одному индивидуальному соединению, а нескольким окрашенным веществам, образование которых зависит от природы исходной аминокислоты. [31]
 |
Схема процесса получения L-аминокислот, добавляемых в корм животным. [32] |
Каждая молекула аминокислоты может существовать в двух формах, одна из которых является зеркальным отображением другой, как правая и левая рука. Все существующие в природе аминокислоты являются L-аминокислотами. Гораздо легче получить аминокислоты путем химического синтеза, чем выделять их из клеток, однако синтезированные аминокислоты образуются в виде смеси равных количеств D - и L-изомеров. [33]
 |
Активный центр фермента ( схема ( по Малеру и Кордесу. [34] |
Она сводится к определению природы аминокислот, их последовательности и взаиморасположения в активном центре. [35]
Остаток ароматической аминокислоты может быть доступен для растворителя и подвергаться воздействию среды, или он может быть маскирован в глубине глобулы, т.е. окружен боковыми цепями других аминокислот. В зависимости от состава среды или природы соседних аминокислот в УФ-спектре могут наблюдаться те или иные изменения, которые измеряют с помощью дифференциальной спектрофотометрии между нативным и денатурированным или гидролизованным белком или же снятием спектров в различных средах. [36]
В случае смеси двух N-карбоксиангидридов образуется сополимер аминокислот. Распределение аминокислот в цепи при этом оказывается не статистическим, а определяется природой аминокислот. На основе тех же принципов могут быть получены полимеры, состоящие из повторяющихся коротких последовательностей аминокислот. [37]
К таким экспериментам также следует отнестись критически, особенно в тех случаях, когда после однократного добавления одной какой-либо аминокислоты авторы измеряли активность протеина плазмы. Действительно, введенв ая аминокислота не только включается в состав протеинов, но одновременно, в зависимости от природы аминокислоты, может участвовать и в других процессах. [38]
У большинства животных молекула ( 3 - МСГ состоит из 18 остатков аминокислот; кроме того, имеются видовые различия, касающиеся природы аминокислоты в положениях 2, 6 и 16 полипептидной цепи гормона. [39]
С-потенциал равен О, для гидрофобных золей наступает в тот момент, когда число зарядов ионов-коагуляторов, проникших за плоскость скольжения в, адсорбционный слой мицеллы, становится равным числу зарядов противоположного знака потенциалобразующих ионов, причем момент этот всецело зависит от концентрации электролита-коагулятора и лишь косвенным образом связан с значением рН среды. При этом особенно интересно и важно то, что значение рН, отвечающее нейтральному-изоэлектри-ческому-состоянию белковой макромолекулы, отнюдь не является постоянным и равным 7, а зависит от природы аминокислот, образующих белок. [40]
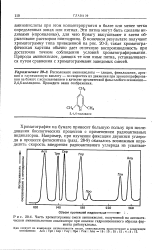 |
Часть хроматограммы смеси аминокислот, полученной на автоматическом аминокислотном анализаторе при анализе гидролизованного образца фермента рибонуклеазы. [41] |
Эти пятна могут быть сделаны видимыми ( проявлены), для чего бумагу высушивают и затем обрызгивают раствором нингидрина. В конечном результате получают хроматограмму типа приведенной на рис. 20 - 3; такая хроматогра-фическая картина обычно дает отличную воспроизводимость при достаточно точном соблюдении условий хроматографирования. Природа аминокислот, дающих те или иные пятна, устанавливается путем сравнения с хроматограммами заведомых смесей. [42]
Среди встречающихся в природе аминокислот ее дает только цистеин. Арнольд рекомендует при подщелачивании раствора заменить NaOH или КОН аммиаком. При прибавлении уксусной кислоты раствор быстро обесцвечивается. [43]
Известны многочисленные виды аминокислот, но биологически важными среди них являются преимущественно первичные ос-аминокислоты наряду с некоторыми вторичными а-аминокисло-тами. Аминокислоты играют гораздо меньшую роль. Большинство встречающихся в природе аминокислот имеет строение типа RCH ( NH2) CO2H, и наше внимание будет сосредоточено именно на этом классе соединений. [44]
Фильтровальная бумага после разделения смеси опрыскивается раствором реагента, дающего цветную реакцию. В качестве такого реагента обычно применяют раствор нингидрина в бутиловом спирте. Окраска варьирует от голубой до оранжевой, в зависимости от природы аминокислот. [45]
Страницы: 1 2 3 4